Trifenyylifosfiinioksidi
Trifenyylifosfiinioksidi (C18H15OP) on orgaaninen fosforiyhdiste, jota syntyy usein sivutuotteena kemiallisessa synteesissä käytettäessä trifenyylifosfiinia. Ainetta käytetään yhdisteiden kiteyttämiseen ja palamisen hidastamiseen.[3]. Trifenyylifosfiini muodostaa myös kompleksiyhdisteitä useiden metallien kanssa.
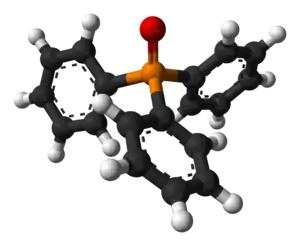
| Trifenyylifosfiinioksidi | |
|---|---|
 |
|
 |
|
| Tunnisteet | |
| CAS-numero | |
| IUPAC-nimi | Difenyylifosforyylibentseeni |
| SMILES | C1=CC=C(C=C1)P(=O)(C2=CC=CC=C2)C3=CC=CC=C3 [1] |
| Ominaisuudet | |
| Kemiallinen kaava | C18H15OP |
| Moolimassa | 278,27 g/mol |
| Sulamispiste | 156,5 °C [2] |
| Kiehumispiste | > 360 °C |
| Liukoisuus | 62,8 mg/l (20 °C) [2] |
Ominaisuudet ja rakenne
Huoneenlämpötilassa trifenyylifosfiinioksidi on valkoista tai ruskehtavaa kiinteää ainetta. Se on vain hieman liukoista veteen, mutta liukenee paremmin muihin poolisiin liuottimiin kuten metanoliin ja tetrahydrofuraaniin.[2][3]
Trifenyylifosfiinioksidikiteillä on kaksi päämuotoa, monokliininen ja ortorombinen. Rakenne ei kuitenkaan ole täysin jäykkä vaan fenyylirenkaiden ja fosforin välinen sidos pääsee kiertymään. Sidoskulmien vaihtelun vuoksi trifenyylifosfiinioksidi esiintyy 62 erilaisessa kidekonformaatiossa.[4]
Trifenyylifosfiinioksidi kiteytyy itse helposti. Yhdisteen fosforiatomi ottaa melko helposti vastaan protonin. Lisäksi yhdisteen happiatomi muodostaa vetysidoksia trifenyylifosfiinioksidikomplekseissa, mikä tekee myös yhdisteestä käyttökelpoisen muiden yhdisteiden kiteyttämisessä.[5]
Trifenyylifosfiinioksidi muodostaa kompleksiyhdisteitä useiden metallikationien kanssa. Näitä ovat muun muassa lantanidit, skandium, yttrium, beryllium, rodium ja tina.[6]
Trifenyylifosfiinioksidi orgaanisen synteesin sivutuotteena
Trifenyylifosfiinioksidia syntyy useiden orgaanisten reaktioiden sivutuotteena, kun reaktioissa käytetään trifenyylifosfiinia. Tällaisia reaktioita ovat esimerkiksi Wittigin, Staudigerin ja Mitsunoboun reaktiot. Trifenyylifosfiinioksidia syntyy myös, kun alkoholeista syntetisoidaan alkyylihalogenideja.[7]
- PPh3 + CBr4 + RCH2OH → OPPh3 + RCH2Br + HCBr3
Trifenyylifosfiinioksidin voi pelkistää takaisin trifenyylifosfiiniksi trikloorisilaanin avulla. Pelkistys voi tapahtua joko amiinikatalyytin kanssa tai ilman sitä. Voidaan käyttää myös poolittomia liuottimia, mutta nekään eivät ole välttämättömiä.[8]
- Ph3PO + SiHCl3 → PPh3 + 1/n (OSiCl2)n + HCl
Trifenyylifosfiinioksidi on melko vaikea erottaa halutuista tuotteista. Käytettäessä kromatografisia erotusmenetelmiä poistettavan trifenyylifosfiinioksidin mukana saataa poistua myös toivottuja yhdisteitä. Aine voidaan saostaa kiteiksi lisäämällä tuotteiden seokseen eetteriä. Voidaan myös käyttää muita fosfiiniyhdisteitä, jotka ovat helpommin poistettavia synteesin aikana.[9]
Lähteet
- Triphenylphosphine oxide – Substance summary NCBI. Viitattu 28. maaliskuuta 2009.
- Physical properties: Triphenylphosphine oxide NLM Viitattu 28.3.2009
- TPPO (Triphenylphosphine oxide Arkema Inc.. Viitattu 28.3.2009. (englanniksi)
- Jenny P. Glusker, Mitchell Lewis, Miriam Rossi: Crystal Structure Analysis for Chemists and Biologists, s. 542. John Wiley and Sons, 1994. ISBN 978-0-471-18543-7. Kirja Googlen teoshaussa (viitattu 28.3.2009). (englanniksi)
- Margaret C. Etter, Paul W. Baures: Triphenylphosphine oxide as a crystallization aid. J. Am. Chem. Soc, 1988, 110. vsk, nro 2, s. 639–640. American Chemical Society. Artikkelin verkkoversio. Viitattu 28.3.2009. (englanniksi)
- J. C. Tebby, D. W. Allen: Organophosphorus Chemistry, s. 32. Royal Society of Chemistry, 2005. ISBN 978-0-85404-339-2. Kirja Googlen teoshaussa (viitattu 28.3.2009). (englanniksi)
- Appel Reaction Organic Chemistry Portal. Viitattu 28. maaliskuuta 2009.
- John Y. Lee,: Process for preparing tertiary phosphines freepatentsonline.com. Viitattu 28.3.2009.
- Patrick J. Murphy: Organophosphorus Reagents, s. 154. Oxford University Press, 2004. ISBN 9780198502623. Kirja Googlen teoshaussa (viitattu 28.3.2009). (englanniksi)