Alkeenit
Alkeenit ovat hiiliatomien välisen kaksoissidoksen sisältäviä hiilivetyjä. Suoraketjuisten alkeenien eli n-alkeenien yleinen kaava on CnH2n. Alkeeneja kutsutaan toisinaan myös olefiineiksi (’öljyä muodostava’), mutta alkeeni on suositeltavampi nimitys.[1] Yksinkertaisimmat alkeenit, eteeni (C2H4) ja propeeni (C3H6), ovat tärkeimmät teollisesti valmistetut orgaaniset kemikaalit.[1]

Nimeäminen
| Nimi | Molekyylikaava | CAS-numero |
|---|---|---|
| Eteeni | C2H4 | 74-85-1 |
| Propeeni | C3H6 | 115-07-1 |
| Buteeni | C4H8 | 106-98-9 |
| Penteeni | C5H10 | 109-67-1 |
| Hekseeni | C6H12 | 592-41-6 |
| Hepteeni | C7H14 | 592-76-7 |
| Okteeni | C8H16 | 111-66-0 |
| Noneeni | C9H18 | 124-11-8 |
| Dekeeni | C10H20 | 872-05-9 |
| Undekeeni | C11H22 | 821-95-4 |
| Dodekeeni | C12H24 | 112-41-4 |
| Tridekeeni | C13H26 | 2437-56-1 |
| Tetradekeeni | C14H28 | 1120-36-1 |
| Pentadekeeni | C15H30 | 13360-61-7 |
| Heksadekeeni | C16H32 | 629-73-2 |
| Heptadekeeni | C17H34 | 6765-39-5 |
| Oktadekeeni | C18H36 | 112-88-9 |
| Nonadekeeni | C19H38 | 18435-45-5 |
| Eikoseeni | C20H40 | 3452-07-1 |
| Heneikoseeni | C21H42 | 27400-79-9 |
| Dokoseeni | C22H44 | 1599-67-3 |
| Trikoseeni | C23H46 | 56924-46-0 |
| Tetrakoseeni | C24H48 | 10192-32-2 |
| Pentakoseeni | C25H50 | 16980-85-1 |
| Heksakoseeni | C26H52 | 18835-33-1 |
| Heptakoseeni | C27H54 | 15306-27-1 |
| Oktakoseeni | C28H56 | 18835-34-2 |
| Nonakoseeni | C29H58 | 77046-61-8 |
| Triakonteeni | C30H60 | 18435-53-5 |
| Hentriakonteeni | C31H62 | 18435-54-6 |
| Dotriakonteeni | C32H64 | 18435-55-7 |
| Tritriakonteeni | C33H66 | 61868-11-9 |
| Tetratriakonteeni | C34H68 | 61868-12-0 |
| Pentatriakonteeni | C35H70 | 61868-13-1 |
| Heksatriakonteeni | C36H72 | 61868-14-2 |
| Heptatriakonteeni | C37H74 | 61868-15-3 |
| Oktatriakonteeni | C38H76 | 61868-16-4 |
| Nonatriakonteeni | C39H78 | 61868-17-5 |
| Tetrakonteeni | C40H80 | 61868-18-6 |
Alkeenit nimetään samaan tapaan kuin alkaanitkin korvaamalla aani-pääte eeni-päätteellä. Yhdistettä nimettäessä etsitään pisin kaksoissidoksen sisältävä hiiliketju, joka edelleen numeroidaan siitä päästä, josta kaksoissidos saa pienimmän mahdollisen luvun.[1] Jos yhdisteessä on kuitenkin hydroksyyliryhmä (-OH), numeroidaan alkeeni niin, että hydroksyyli saa pienimmän luvun.[2] Tällöin yhdisteen perheestä käy ilmi molemmat funktionaaliset ryhmät (esimerkki: 3-pente-2-oli). Mikäli hydroksyyliryhmättömän alkeenin kaksoissidos saa saman luvun kummastakin päästä, numeroidaan yhdiste niin, että yhdisteen substituentti (muu kuin hydroksyyli) saa pienimmän mahdollisen luvun. Substituentit listataan paikkanumeron kanssa aakkosjärjestyksessä yhdisteen eteen. Kaksoissidoksen paikan ilmaiseva luku kirjoitetaan puolestaan yhdisteen ”perheen” eteen (esimerkiksi 2-buteeni). Mikäli kaksoissidoksia on useampia, niiden luvut erotetaan pilkulla, ja yhdisteen nimen pääte on dieeni, trieeni jne. kaksoissidosten lukumäärän mukaan.[1]
Sykloalkeenien nimeäminen aloitetaan kaksoissidoksesta niin, että kaksoissidos on ensimmäisen ja toisen hiiliatomin välissä.[1] Siten yksiarvoisen sykloalkeenin kaksoissidoksen paikkaa ei tarvitse erikseen kirjoittaa.
C=C-sidoksen sisältävät ryhmät
Substituentti =CH2 tunnetaan metyleeniryhmänä, H2C=CH– vinyyliryhmänä ja H2C=CHCH2 allyyliryhmänä.[1]

Kaksoissidos

Kaksoissidokseen osallistuva hiiliatomi on sp2-hybridisoitunut, jolloin muodostuneet kolme sp2-orbitaalia ovat samassa tasossa noin 120° kulmassa toisiinsa nähden. Hiilen neljäs orbitaali, p-orbitaali, on tuohon tasoon kohtisuorassa. Kaksoissidos koostuu sp2-orbitaalien σ-sidoksesta ja p-orbitaalien π-sidoksesta.[1] Kaksoissidos on vahvempi kuin yksinkertainen kovalenttinen sidos: eteenin kaksoissidoksen sidosenergia on 605 kJ/mol, kun vastaavasti etaanin yksinkertaisen sidoksen sidosenergia on 368 kJ/mol.[2] Kaksoissidos (134 pm) on hieman yksinkertaista sidosta (150 pm) lyhyempi.[2]
Hiiliatomit kaksoissidoksessa eivät voi kiertyä toistensa suhteen π-sidoksen vuoksi. Kiertyminen edellyttäisi π-sidoksen rikkomiseen vaadittavaa energiaa (268 kJ/mol).[1] Esimerkiksi etaanin kiertyminen σ-sidoksen ympäri edellyttää energiaa vain 12 kJ/mol.
Alkeenin stabiilisuuteen korreloi kaksoissidoksen hiiliatomeihin liittyneiden substituenttien (jokin muu kuin vetyatomi) lukumäärä siten, että useampi substituentti merkitsee pysyvämpää rakennetta. Eli stabiilisuuden kannalta pätee:[1]
- tetrasubstituoitu > trisubstituoitu > disubstituoitu > monosubstituoitu > ei substituentteja (eteeni)
Stabiilisuus on seurausta hyperkonjugaatiosta eli kaksoissidoksen hiilien välisen π-sidosorbitaalin ja substituentin (vedyn) ja hiilen välisen σ-sidosorbitaalin vuorovaikutuksesta sekä vahvemmista kovalenttisista sidoksista hiiliatomien välillä. Sidos sp3- ja sp2-hybridisoituneen hiiliatomin välillä on vahvempi kuin sidos kahden sp3-hiilen välillä.[1] Täten ratkaisevaa on myös kaksoissidoksen paikka molekyylissä.
Tyydyttymättömyys
Alkeeniin on kaksoissidoksen vuoksi liittyneenä vähemmän vetyä vastaavaan alkaaniin verrattuna. Sen vuoksi alkeeneja kutsutaan tyydyttymättömiksi hiilivedyiksi.[1] Yhdisteen ”tyydyttymättömyysaste” tarkoittaa yhdisteestä lähteneitä vetyjä H2 verrattuna vastaavaan suoraketjuiseen alkaaniin CnH2n+2.[1] Siten yksi kaksoissidos tai rengasrakenne tarkoittaa tyydyttymättömyysastetta 1. Yhdisteen sisältämä halogeeni lisää tyydyttymättömyysastetta puolella yksiköllä. Yhdisteeseen yksinkertaisin sidoksin liittynyt happi ei vaikuta yhdisteen tyydyttymättömyysaseeseen, sillä sen sidokset johtavat lopulta hiileen tai vetyyn. Happea ei siten tyypillisesti tarvitse huomioida yhdisteen tyydyttymättömyysastetta laskiessa. Yksinkertaisin sidoksin liittynyt typpi puolestaan vähentää yhdisteen tyydyttymättömyysastetta, sillä se muodostaa kolme sidosta. Yleensä typpi vastaa kahta vetyä yhden vedyn sijalla, eli se pienentää yhdisteen tyydyttymättömyysastetta puolella yksiköllä.
Cis-trans-isomeria
Alkeeneilla esiintyy cis-trans-stereoisomeriaa jäykän kaksoissidoksen vuoksi, jos kaksoissidos on vähintään disubstituenttinen. Disubstituenttisen kaksoissidoksen substituentit voivat olla kaksoissidoksen samalla (cis-isomeeri) tai eri puolella (trans-isomeeri). Cis-trans-isomeria ei ole mahdollinen, jos toisen kaksoissidokseen osallistuvan hiiliatomin substituentit ovat identtiset.[1]
Yhdisteen muuntuminen cis-muodosta trans-muotoon tai päinvastoin ei tapahdu spontaanisti, mutta se voidaan katalysoida vahvalla hapolla.[1]
Alkeenien trans-isomeerit ovat pysyvämpiä kuin cis-isomeerit. Alkeenien cis-isomeereilla substituenttien välillä ilmenee steeristä jännitystä ja ne ovat siksi suurienergiaisempia.[1] Aineen cis- ja trans-isomeerien suhdetta voidaan tutkia isomeerien energiaeroa hyödyntämällä niiden palamislämmöstä:[1] paljon cis-muotoa sisältävä alkeeni vapauttaa palaessaan enemmän lämpöenergiaa kuin paljon trans-muotoa sisältävä. Toinen vaihtoehto on hydrogenoida alkeenia palladium- tai platinakatalyytin avulla ja tarkkailla siitä vapautuvaa lämpöä.[1]
E,Z-isomeria
Mikäli kaksoissidos on luonteeltaan tri- tai tetrasubstituenttinen, on stereoisomeria ilmaistava yleisemmin E,Z-järjestelmällä sekvenssisääntöjen mukaisesti. Sekvenssisäännöt luokittelevat substituentit tärkeysasteisiin, ja lopputuloksesta käy ilmi, ovatko hiiliatomien tärkeimmät substituentit samalla puolella (Z-muoto, saks. zusammen ’yhdessä’) vai eri puolilla (E-muoto, saks. entgegen ’vastakkain’) kaksoissidosta.
Sekvenssisäännöt (Cahn–Ingold–Prelogin säännöt):
- Käsitellessä kumpaakin kaksoissidoksen hiilistä erikseen, hiiliatomeista lähtevät atomit saavat atomiluvun mukaan kasvavan tärkeysasteen.[1] Yleisimpien orgaanisten atomien tärkeysasteet ovat siten: vety 1, hiili 6, typpi 7, happi 8, kloori 17, bromi 35. Esimerkiksi, jos kaksoissidoksen toiseen hiiliatomiin on liittyneenä hiili ja happi, on happiatomi tai happilähtöinen substituentti tärkeämpi.
- Jos ensimmäiset kaksoissidoksen hiilestä lähtevät atomit ovat samoja, tarkastellaan toisia, kolmansia, neljänsiä jne. atomeja, kunnes eroavaisuus toisen hyväksi löytyy.[1]
- Kaksoissidos on verrattavissa kahteen ja kolmoissidos kolmeen yksinkertaisella kovalenttisella sidoksella sitoutuneeseen atomiin.[1] Esimerkiksi hiilestä lähtevä kaksoissidos happeen (–C=O) on verrattavissa kahden hiilen väliseen happisiltaan (–C–O–C).
Valmistaminen
Lämpökrakkaus
Eteeniä, propeenia ja buteenia valmistetaan lämpökrakkaamalla maakaasua (C1–C4-alkaaneja) tai suoratislettä (C4–C8-alkaaneja).[1] Lämpökrakkaus tapahtuu ilman katalyyttejä korkeissa, jopa 900 °C:n lämpötiloissa.
Eliminaatioreaktio
Alkeeneja voidaan valmistaa eliminaatioreaktiolla alkyylihalideista (dehydrohalogenointi) ja alkoholeista (dehydraatio). Alkyylihalidin dehydrohalogenointi eli vetyhalidin poistuminen tapahtuu yleisesti vahvan emäksen vaikutuksesta.[1] Alkoholin dehydraatio eli vesimolekyylin poistuminen tapahtuu puolestaan usein vahvan hapon vaikutuksesta.[1]
Hyödyntäminen
Eteenistä ja propeenista voidaan teollisesti syntetisoida lukuisia eri kemikaaleja:[1]
| Eteeni | Propeeni |
|---|---|
| etanoli | isopropyylibentseeni |
| asetaldehydi | isopropyylialkoholi |
| etaanihappo | polypropeeni |
| vinyylikloridi | propyleenioksidi |
| vinyyliasetaatti | |
| polyeteeni | |
| etyleenioksidi | |
| etyleeniglykoli | |
| 1,2-etyleenidikloridi |
Reaktiot
Kaksoissidos on osallisena useimpiin alkeenien reaktioihin.
Additioreaktio
Alkeenin additioreaktio voidaan esittää yleisesti:
Markovnikovin säännön mukaisesti substituentti liittyy aina siihen hiiliatomiin, jossa on ennestään enemmän muita substituentteja.
Hydrogenointi
Hydrogenointi on additioreaktio, jossa vetymolekyyli H2 liittyy alkeenin kaksoissidokseen.[2] Tällöin kaksoissidos muuttuu yksinkertaiseksi sidokseksi.
Esimerkiksi eteenin hydrogenointi etaaniksi:
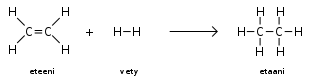
Hydrogenointireaktiot ovat luonteeltaan eksotermisia, eli ne vapauttavat lämpöä. Hydrogenointireaktiossa käytetään usein katalyyttiä reaktion nopeuttamiseksi. Katalyytteinä voidaan käyttää platinaa, palladiumia, nikkeliä tai rodiumia. Platina on yleisimmin käytetty katalyytti.[2] Katalysoidussa alkeenin hydrogenoinnissa alkeeni liuotetaan ensin esimerkiksi etanoliin, etaanihappoon tai heksaaniin. Liuos tuodaan tämän jälkeen kosketuksiin metallikatalyytin kanssa, ja katalyysi tapahtuu heterogeenisesti metallin pinnalla.[2]
Vetyhalidien elektrofiilinen additio
Vetyhalidit (vetykloridi HCl, vetybromidi HBr, vetyjodidi HI ja vetyfluoridi HF) tuottavat alkeenien kanssa reagoidessaan alkyylihalideja:
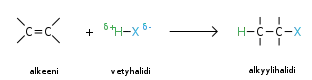
Tietyn vetyhalidin reaktiivisuus on verrannollinen sen happamuuteen eli protoninluovutuskykyyn.[2] Reaktiivisuus on edelleen verrannollinen reaktionopeuteen. Koska vetyjodidi on vetyhalideista happamin, additioreaktio alkeenin kanssa käy siltä muita vetyhalideja nopeammin.
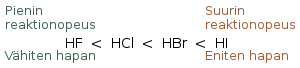
Vetyhalidin elektrofiilinen additio on kaksivaiheinen ja sillä on kaksi siirtymäkompleksia. Ensimmäisessä vaiheessa vetyhalidin elektrofiilinen vety yhtyy alkeenin nukleofiiliseen π-sidokseen, ja alkeenista muodostuu karbokationi-intermediaatti halogeenin jäädessä anioniksi. Seuraavassa vaiheessa halogeenianioni jakaa elektroniparinsa karbokationin kanssa, ja muodostuu σ-sidos hiilen ja halogeenin välille.[1]

Halogeenien additio
Halogeenit reagoivat alkeenien kanssa muodostaen 1,2-dihaloalkaaneja. 1,2-dihaloalkaanien halogeenit asettuvat aina yhdisteen vastakkaisille puolille, ja muodostuva yhdiste on anti-stereokemiallinen.[1] Esimerkiksi bromin Br2 ja syklopenteenin reaktiossa syntyy vain trans-1,2-dibromosyklopentaania. Reaktiosta muodostuvien yhdisteiden anti-stereokemiallisuus selittyy haloniumioni-välituotteen muodostumisella.[1] Haloniumioni (esim. bromonium-ioni) estää toisen halogeeniatomin liittymisen yhdisteen samalle puolelle.
Happokatalysoitu hydrataatio
Kun alkeeni reagoi veden kanssa hapon läsnä ollessa, saadaan alkoholeja. Esimerkiksi etanolia valmistetaan eteenistä hydrataatiolla:

Katalyyttinä toimiva happoliuos on laimea. Usein käytetään 50-prosenttista rikkihapon vesiliuosta.[2] Liuoksen vesipitoisuus on verrannollinen saatavan lopputuotteen määrään tasapainoreaktiossa Le Châtelier’n periaatteen mukaisesti.[2] Happokatalysoitu dehydraatio on happokatalysoidun hydraation käänteisreaktio, ja siinä käytettävän happoliuoksen happokonsentraatio on suuri.
Alkeenin happokatalysoitu hydraatio on elektrofiilinen reaktio. Reaktion ensimmäisessä vaiheessa alkeenista tulee karbokationi vesiliuoksen hydroniumionin vedyn liityttyä kaksoissidokseen.[2]

Seuraavassa vaiheessa vesimolekyylin happi jakaa vapaan elektroniparin elektrofiiliselle hiilelle. Karbokationi muuttuu siten oksoniumioniksi.[2]
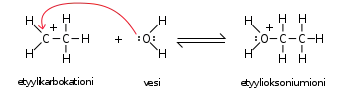
Alkoholi jää jäljelle oksoniumionin luovutettua protonin vedelle.[2]

Etanolia lukuun ottamatta happokatalysoidulla hydraatiolla tuotettavat alkoholit ovat sekundaarisia tai tertiaarisia, sillä Markovnikovin säännön mukaisesti hydroksidisubstituentti liittyy siihen kaksoissidoksen hiileen, jossa on jo ennestään enemmän (muun muassa alkyyli-) substituentteja.
Hapettuminen
Alkeenien hapettumisessa reaktiotuotteena on hiiliatomien ja happiatomin muodostama rengas, joka on hyvin reaktiokykyinen. Hapettimet, kuten kaliumpermanganaatti KMnO4 ja otsoni O3, hapettavat kaksoissidoksen joko niin, että kaksoissidoksen π-sidos aukeaa tai siten, että kaksoissidos katkeaa. Emäksisessä liuoksessa C=C-sidos hapettuu KMnO4:lla 1,2-dialkoholiksi eli dioliksi, joka on syn-reaktiotuote eli cis-isomeeri. Esimerkiksi sykloheksaania hapetettaessa saadaan cis-1,2-sykloheksadiolia. Otsoni O3 hapettaa alkeenit purkamalla hiiliatomien välisen kaksoissidoksen. Reaktioissa syntyvä otsonidi hydrolysoituu helposti. Tuotteena muodostuu karbonyyliyhdisteitä: aldehydejä, ketoneja tai karboksyylihappoja.
Polymerointi
Eräs alkeenien tärkeimpiä teollisia reaktiota on polymerointi, jossa pienet alkeenimolekyylit liittyvät toisiinsa muodostaen yhden makromolekyylin eli polymeerin. Esimerkiksi eteenistä voidaan valmistaa polymeeriä, polyeteeniä.
Lähteet
- John McMurry: Organic Chemistry (5th edition), s. 188–231. Brooks/Cole, 2000. ISBN 0-534-37366-6. (englanniksi)
- Francis A. Carey: Organic Chemistry (4th edition), s. 167–258. McGraw-Hill, 2000. ISBN 0-07-290501-8. (englanniksi)
Aiheesta muualla
 Kuvia tai muita tiedostoja aiheesta Alkeenit Wikimedia Commonsissa
Kuvia tai muita tiedostoja aiheesta Alkeenit Wikimedia Commonsissa
| Alkaanit |
| ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Alkeenit |
| ||||||||||||||||||||||||
| Alkyynit |
|
