Meldrumin happo
Meldrumin happo eli 2,2-dimetyyli-1,3-dioksaani-4,6-dioni (C6H8O4) on heterosyklisiin dilaktoneihin kuuluva orgaaninen yhdiste. Yhdistettä käytetään yleisesti reagenssina orgaanisen kemian synteeseissä.
| Meldrumin happo | |
|---|---|
 |
|
| Tunnisteet | |
| CAS-numero | |
| IUPAC-nimi | 2,2-dimetyyli-1,3-dioksaani-4,6-dioni |
| SMILES | CC1(OC(=O)CC(=O)O1)C[1] |
| Ominaisuudet | |
| Kemiallinen kaava | C6H8O4 |
| Moolimassa | 144,124 g/mol |
| Sulamispiste | 92–95 °C (hajoaa)[2] |
| Liukoisuus | Liukenee veteen |
Rakenne ja ominaisuudet
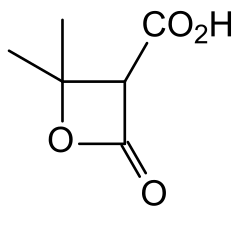
Ensimmäisen kerran Meldrumin happoa syntetisoi Andrew Norman Meldrum vuonna 1908 asetonin ja malonihapon välisellä reaktiolla Meldrum arveli syntetisoimansa yhdisteen rakenteen olevan β-hydroksi-isopropyylimalonihapon β-laktonin.[3][4] Vuonna 1948 David Davidson ja Sidney Bernhard osoittivat yhdisteen todellisuudessa kuitenkin olevan 2,2-dimetyyli-1,3-dioksaani-4,6-dionia perustuen tarkempaan tietämykseen yhdisteen reaktiivisuudesta[4][5].

Meldrumin happo on huoneenlämpötilassa väritöntä kiteistä ainetta. Yhdiste liukenee hyvin sekä veteen että poolisiin orgaanisiin liuottimiin. Meldrumin happo on laktoniksi poikkeuksellisen voimakas happo ja sen pKa-arvo vesiliuoksessa on 4,83 eli sen on vahvuudeltaan etikkahapon luokkaa. Eritysen poikkeukselliseksi tämän tekee se, että protonin luovuttaa hiiliatomi. Meldrumin happo esiintyy neutraalissa muodossa venekonformaatiossa ja esteriryhmät sijaitsevat syn-asemassa toisiinsa nähden eli samaan sunntaan molekyylitasoon verrattuna. Yhdisteen deprotonoituessa tapahtuu konformaation muutos, joka on energeettisesti edullinen johtuen suotuisammista vuorovaikutuksista eri molekyyliorbitaalien välillä ja anomeerisesta efektistä.[6][7]
Valmistus ja käyttö
Meldrumin happoa voidaan valmistaa malonihapon ja asetonin välisellä reaktiolla etikkahappoanhydridin läsnä ollessa. Yhdistettä voidaan syntetisoida myös dietyylimalonaatista kaksivaiheisella reaktiolla tai isoprenyyliasetaatista rikkihapon avulla.[2][8][9]
Meldrumin happo on hyödyllinen molekyyli orgaanisen kemian synteeseissä erityisesti kaksi tai kolme hiiliatomia sisältävänä niin kutsuttuna syntonina. Yhdiste reagoi muun muassa Knoevenagel-kondensaatiolla ja sen voidaan alkyloida tai asyloida. Alkyloitujen tai asyloitujen Meldrumin hapon johdannaisten reaktio alkoholien kanssa on kätevä tapa muodostaa malonihapon monoestereitä ja β-ketoestereitä. Lisäksi yhdiste soveltuu monien heterosyklisten yhdisteiden synteesiin ja siitä on syntetisoitu erityisesti pyridiini-, pyridoni-, pyrimidiini- ja triatsiinijohdannaisia. Melrumin hapon ja sen johdannaisten pyrolyysissä muodostuu keteenejä, jotka ovat myös hyödyllisiä synteessisen kemian välituotteita.[2][4][8][9][10][11]
Lähteet
- 2,2-Dimethyl-1,3-dioxane-4,6-dione – Substance summary PubChem. NCBI. Viitattu 22.8.2015.
- Harald Strittmatter, Stefan Hildbrand & Peter Pollak: Malonic Acid and Derivatives, Ullmann's Encyclopedia of Industrial Chemistry, John Wiley & Sons, New York, 2007. Viitattu 22.8.2015
- Andrew Norman Meldrum: LIV.—A β-lactonic acid from acetone and malonic acid. Journal of the Chemical Society, Transactions, 1908, 93. vsk, s. 598–601. Artikkelin verkkoversio. Viitattu 22.8.2015. (englanniksi)
- Victoria V. Lipson & Nikolay Yu. Gorobets: One hundred years of Meldrum’s acid: advances in the synthesis of pyridine and pyrimidine derivatives. Molecular Diversity, 2009, 13. vsk, nro 4, s. 399–419. Artikkelin verkkoversio. Viitattu 22.8.2015. (englanniksi)
- David Davidson & Sidney A. Bernhard: The Structure of Meldrum's Supposed β-Lactonic Acid. Journal of the American Chemical Society, 1948, 70. vsk, nro 10, s. 3426–3428. Artikkelin verkkoversio. Viitattu 22.8.2015. (englanniksi)
- Michael B. Smith & Jerry March: March's Advanced Organic Chemistry, s. 340–341. John Wiley & Sons, 2013. ISBN 9780470462591. (englanniksi)
- Satoshi Nakamura, Hajime Hirao & Tomohiko Ohwada: Rationale for the Acidity of Meldrum's Acid. Consistent Relation of C−H Acidities to the Properties of Localized Reactive Orbital. The Journal of Organic Chemistry, 2004, 69. vsk, nro 13, s. 4309–4316. Artikkelin verkkoversio. Viitattu 22.8.2015. (englanniksi)
- Peter Pollak & Gérard Romeder: Malonic Acid and Derivatives, Kirk-Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, New York, 2000. Viitattu 22.8.2015
- Osamu Yonemitsu, Ken-ich Elghanian & Amy C. Hart: 2,2-Dimethyl-1,3-dioxane-4,6-dione, e-EROS Encyclopedia of Reagents for Organic Synthesis, John Wiley & Sons, New York, 2010. Teoksen verkkoversio Viitattu 22.8.2015
- Romano V. A. Orru,Eelco Ruijter: Synthesis of Heterocycles Via Multicomponent Reactions I, s. 64–66. Springer, 2010. ISBN 978-3-642-12674-1. Kirja Googlen teoshaussa (viitattu 22.8.2015). (englanniksi)
- Serban C. Moldoveanu: Pyrolysis of Organic Molecules, s. 604. Elsevier, 2009. ISBN 9780444531131. Kirja Googlen teoshaussa (viitattu 22.8.2015). (englanniksi)
