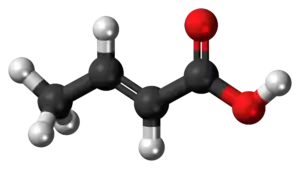
Krotonihappo
Krotonihappo (C4H6O2) on tyydyttymättömiin karboksyylihappoihin kuuluva orgaaninen yhdiste. Yhdistettä käytetään orgaanisen kemian synteeseissä muun muassa lääkkeiden, polymeerien ja muiden kemikaalien valmistukseen.
| Krotonihappo | |
|---|---|
 |
|
 |
|
| Tunnisteet | |
| CAS-numero | |
| IUPAC-nimi | But-2-eenihappo |
| SMILES | CC=CC(=O)O[1] |
| Ominaisuudet | |
| Kemiallinen kaava | C4H6O2 |
| Moolimassa | 86,088 g/mol |
| Tiheys | 1,018[2] g/cm³ |
| Sulamispiste | 71,5–71,7 °C[2] |
| Kiehumispiste | 185 °C[2] |
| Liukoisuus | Veteen 76,1 g/l (25 °C)[3] |
Ominaisuudet
Huoneenlämpötilassa krotonihappo on valkoista tai kellertävää kiteistä ainetta, jolla on voimakkaasti pistävä haju. Yhdisteellä esiintyy cis-trans-isomeria ja trans-isomeeri on termodynaamisesti stabiilimpi. Cis-isomeeria kutsutaan myös isokrotonihapoksi. Krotonihappo voi isomeroitua isokrotonihapoksi kuumennettaessa noin 125 °C:n lämpötilaan. Edelleen kuumennettaessa noin 180 °C:n lämpötilaan tapahtuu isomeroituminen uudelleen krotonihapoksi. Krotonihappo liukenee hyvin veteen sekä useisiin orgaanisiin liuottimiin kuten etanoliin, dietyylieetteriin, asetoniin, etyyliasetaattiin ja tolueeniin. Muiden karboksyylihappojen tavoin krotonihappo on heikko happo ja sen pKa-arvo on 2·10-5. Yhdisteelle tyypillisiä reaktioita ovat muun muassa additioreaktiot, polymerisoitumiset ja esteröitymiset.[2][3][4][5] Luonnossa krotonihappoa on havaittu esiintyvän Texasin savimaaperässä sekä maaöljyssä[3][6].
Krotonihappo on myrkyllistä ja ärsyttää voimakkaasti ihoa, hengitysteitä ja silmiä. Yhdisteelle altistumisesta voi seurata pahoinvointia, kurkkukipua, pääkipua, hengitysvaikeuksia ja iholle tai silmiin joutuessaan syövytysvammoja.[7]
Valmistus ja käyttö
Teollisesti krotonaldehydiä valmistetaan hapettamalla krotonaldehydiä ilmalla tai hapella 20–45 °C:n lämpötilassa. Reaktion ensimmäisessä vaiheessa muodostuu perkrotonihappoa, joka reagoi toisen krotonaldehydimolekyylin kanssa krotonihapoksi. Tuote puhdistetaan kiteyttämällä. Laboratoriomittakaavassa yhdistettä voidaan valmistaa asetaldehydin ja malonihapon välisellä kondensaatioreaktiolla pyridiinin läsnä ollessa, krotonaldehydin fotokemiallisella hapetuksella, allyylialkoholin karbonyloinnilla, kuumentamalla 3-hydroksivoihappoa tai puun kuivatislauksella.[4][3][5][8]
Krotonihappoa käytetään valmistettaessa polymeerejä. Tärkeitä ovat esimerkiksi sen ja vinyyliasetaatin kopolymeerit, joita käytetään muun muassa maaleissa, lakoissa, liimoissa ja sideaineina sekä alkydihartsit. Yhdisteestä valmistettavia estereitä voidaan käyttää muovien ja kumien pehmittiminä. Krotonihaposta valmistetaan myös lääkkeitä kuten krotamitonia ja muita orgaanisia yhdisteitä kuten treoniinia ja A-vitamiinia.[4][3][5][8]
Lähteet
- Crotonic acid – Substance summary PubChem. NCBI. Viitattu 28.5.2016.
- Alén, Raimo: Kokoelma orgaanisia yhdisteitä: Ominaisuudet ja käyttökohteet, s. 389. Helsinki: Consalen Consulting, 2009. ISBN 978-952-92-5627-3.
- Susan Budavari (päätoim.): Merck Index, s. 439–440. 12th Edition. Merck & Co., 1996. ISBN 0911910-12-3. (englanniksi)
- Jürgen Blumenstein, Jens Albert, Rolf P. Schulz & Christian Kohlpaintner: Crotonaldehyde and Crotonic Acid, Ullmann's Encyclopedia of Industrial Chemistry, John Wiley & Sons, New York, 2015. Viitattu 28.5.2015
- Thomas Scott, Mary Eagleson: Concise encyclopedia chemistry, s. 277–278. Walter de Gruyter, 1994. ISBN 978-3110114515. (englanniksi)
- S. Gangolli: The Dictionary of Substances and Their Effects: C, s. 759. RSC Publishing, 1999. ISBN 978-0-85404-813-7. Kirja Googlen teoshaussa (viitattu 28.5.2016). (englanniksi)
- Krotonihapon kansainvälinen kemikaalikortti Viitattu 28.5.2016
- Klaus Weissermel, Hans-Jürgen Arpe: Industrial organic chemistry, s. 186. Wiley-VCH, 2003. ISBN 978-3-527-30578-0. (englanniksi)
