Karbonaatti
Karbonaatti CO32- on anioni, jossa esiintyy hiili- ja happiatomeja. Karbonaateiksi sanotaan myös ioniyhdisteitä, hiilihapon suoloja, joissa karbonaatti-ioni on anionina ja hiilihapon orgaanisia estereitä.[1][2] Esimerkiksi kalsiumkarbonaattia CaCO3 syntyy, kun hiilidioksidia CO2 sitoutuu kalsiumoksidiin CaO.
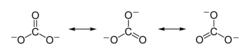
Karbonaatti-ionin resonanssimuodot
Alkalimetallien karbonaatit sekä ammoniumkarbonaatti liukenevat runsaasti veteen, muut karbonaatit ovat hyvin niukkaliukoisia.
Karbonaatteja
- Ammoniumvetykarbonaatti (CH5NO3 / NH4HCO3) CAS-numero 1066-33-7
- Berylliumkarbonaatti (Be2CO3(OH)2 / Be2CO5H2) CAS-numero 66104-24-3
- Dietyylikarbonaatti (C5H10O3 / (C2H5O)2CO) CAS-numero 105-58-8
- Dimetyylikarbonaatti (C3H6O3 / H3COCOOCH3) CAS-numero 616-38-6
- Kaliumkarbonaatti (vedetön) (K2CO3) CAS-numero 584-08-7
- Kalsiumkarbonaatti (CaCO3) CAS-numero 471-34-1
- Kobolttikarbonaatti (CoCO3) CAS-numero 513-79-1
- Kuparikarbonaatti (CuCO3) CAS-numero 12069-69-1
- Litiumkarbonaatti (Li2CO3) CAS-numero 554-13-2
- Lyijykarbonaatti (PbCO3) CAS-numero 598-63-0
- Magnesiumkarbonaatti (MgCO3) CAS-numero 546-93-0
- Natriumbikarbonaatti (NaHCO3) CAS-numero 144-55-8
- Natriumkarbonaatti (vedetön) (Na2CO3) CAS-numero 497-19-8
- Natriumseskvikarbonaattidihydraatti (C2H5Na3O8 / Na2CO3 · NaHCO3·2H2O) CAS-numero 6106-20-3
- Nikkelikarbonaatti (NiCO3) CAS-numero 3333-67-3
- Rauta(II)karbonaatti (FeCO3) CAS-numero 563-71-3
- Talliumkarbonaatti (Tl2CO3) CAS-numero 6533-73-9
Lähteet
- E. M. Karamäki: Epäorgaaniset kemikaalit, s. 518. Kustannusliike Tietoteos, 1983. ISBN 951-9035-61-3.
- Alén, Raimo: Kokoelma orgaanisia yhdisteitä: Ominaisuudet ja käyttökohteet, s. 108. Helsinki: Consalen Consulting, 2009. ISBN 978-952-92-5627-3.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.