Heksafluoriasetoni
Heksafluoriasetoni (C3F6O) on fluorattuihin ketoneihin kuuluva orgaaninen yhdiste. Yhdistettä voidaan käyttää liuottimena sekä lähtöaineena orgaanisen kemian synteeseissä.
| Heksafluoriasetoni | |
|---|---|
 |
|
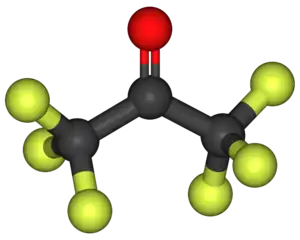 |
|
| Tunnisteet | |
| CAS-numero | |
| IUPAC-nimi | 1,1,1,3,3,3-heksafluoripropan-2-oni |
| SMILES | C(=O)(C(F)(F)F)C(F)(F)F[1] |
| Ominaisuudet | |
| Kemiallinen kaava | C3F6O |
| Moolimassa | 166,03 g/mol |
| Sulamispiste | -122 °C[2] |
| Kiehumispiste | -27,4 °C[3] |
| Liukoisuus | Reagoi veden kanssa |
Ominaisuudet
Heksafluoriasetoni on huoneenlämpötilassa väritöntä kaasua. Paineistettuna se voidaan nesteyttää. Yhdiste reagoi voimakkaasti veden kanssa ja reaktiossa muodostuu stabiili heksafluoriasetonin hydraatti. Reaktio on lämpöä vapauttava eli eksoterminen. Heksafluoriasetoni on myrkyllistä ja ärsyttää voimakkaasti ihoa, silmiä ja hengitysteitä. Aineelle altistumisesta oireina voivat olla yskä, kurkkukipu ja polttava tunne kurkussa ja hengityksen vaikeutuminen. Heksafluoriasetoni voi olla mutageenistä.[2][3][4]
Valmistus ja käyttö
Heksafluoriasetonia voidaan valmisteaa heksaklooriasetonin ja vetyfluoridin välisellä reaktiolla ja katalyyttinä käytetään kromiyhdisteitä. Toinen teollisuudessa käytetty valmistusmenetelmä on Lewis-happojen katalysoima heksafluoripropyleenioksidin isomeroituminen ja tämän prosessin etuna on, että myrkyllisiä sivutuotteita ei muodostu. Laboratorio-olosuhteissa heksafluoriasetonia voidaan valmistaa lähtien heksafluoripropeenista.[3]
Heksafluoriasetonia voidaan käyttää polyamidi-, polyesteri- ja polyasetaalihartsien liuottimena. Yhdistettä käytetään myös heksafluori-isopropanolin, heksafluori-isobuteenin, fluoripolymeerien ja maatalouskemikaalien ja lääkeiaineiden valmistamiseen.[2][3][4]
Lähteet
- Hexafluoroacetone – Substance summary PubChem. NCBI. Viitattu 6.7.2017.
- Richard P. Pohanish: Sittig's Handbook of Toxic and Hazardous Chemicals and Carcinogens, s. 1429. William Andrew, 2011. ISBN 9781437778694. Kirja Googlen teoshaussa (viitattu 6.7.2017). (englanniksi)
- Günter Siegemund, Werner Schwertfeger, Andrew Feiring, Bruce Smart, Fred Behr, Herward Vogel, Blaine McKusick & Peer Kirsch: Fluorine Compounds, Organic, Ullmann’s Encyclopedia of Industrial Chemistry, John Wiley & Sons, New York, 2016. Viitattu 6.7.2017
- Nick H. Proctor, Gloria J. Hathaway, James P. Hughes: Proctor and Hughes' Chemical hazards of the workplace, s. 376-377. Wiley-IEEE, 2004. ISBN 978-0-471-26883-3. Kirja Googlen teoshaussa (viitattu 6.7.2017). (englanniksi)