Glykolihappo
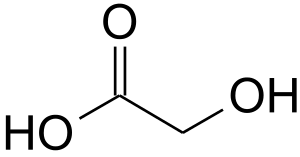
Glykolihappo eli hydroksietikkahappo (C2H4O3) on yksinkertaisin hydroksihapoista eli orgaanisista yhdisteistä, jotka sisältävät sekä karboksyylihapon että alkoholin funktionaalisen ryhmän. Yhdistettä käytetään puhdistusaineissa, polymeeriteollisuudessa, kosmetiikkavalmisteissa ja valmistettaessa muita orgaanisia yhdisteitä.
| Glykolihappo | |
|---|---|
 |
|
 |
|
| Tunnisteet | |
| CAS-numero | |
| IUPAC-nimi | 2-hydroksietikkahappo |
| SMILES | C(C(=O)O)O[1] |
| Ominaisuudet | |
| Kemiallinen kaava | C2H4O3 |
| Moolimassa | 76,052 g/mol |
| Tiheys | 1,49[2] g/cm³ |
| Sulamispiste | 79–80 °C[2] |
| Kiehumispiste | 100 °C (hajoaa)[2] |
| Liukoisuus | Liukenee veteen |
Ominaisuudet
Huoneenlämpötilassa glykolihappo on kiinteätä väritöntä ja hygroskooppista ainetta. Yhdiste liukenee erittäin hyvin veteen ja polaarisiin orgaanisiin liuottimiin kuten etanoliin, metanoliin ja asetoniin. Hiilivetyihin glykolihappo sen sijaan liukenee vain hieman. Yhdiste on keskivahva happo ja sen pKa-arvo on 3,83.[2][3][4]
Glykolihappo sisältää sekä hydroksyylirymän että karboksyyliryhmän ja sille tapahtuu sekä alkoholeille ja karboksyylihapoille tyypillisiä reaktioita. Tällaisia ovat suolojen muodostuminen reaktioissa emästen kanssa, esteröityminen alkoholien kanssa karbokyysliryhmän kautta ja happokloridien kanssa hydroksyyliryhmän kautta ja kompleksien muodostuminen siirtymämetallikationien kanssa. Kuumennettaessa glykolihappo muodostaa esterin itsensä kanssa muodostaen ensin diglykolihappoa ja edelleen pidempiketjuisia oligomeerejä ja lopulta polyglykolihappoa. Voi muodostua myös rengasrakenteisia dimeerejä ja oligomeerejä eli glykolideja.Vetyperoksidi hapettaa yhdisteen rauta(II)suolojen läsnä ollessa glyoksyylihapoksi ja rauta(III)suolojen läsnä ollessa oksaalihapoksi.[2][3][4]
Luonnossa glykolihappoa esiintyy sokeriruo'ossa, sokerijuurikkaassa ja raakojen viinirypäleiden mehussa.[2][3][4] Ihmisen elimistössä glykolialdehydi hapettuu glykolihapoksi.
Valmistus ja käyttö
Ensimmäisen kerran glykolihappoa valmistettiin vuonna 1848 glysiinin ja typpihapokkeen välisellä reaktiolla.[3] Glykolihappoa voidaan valmistaa hydrolysoimalla kloorietikkahappoa emäksisissä olosuhteissa 90–130 °C:n lämpötilassa, jonka jälkeen happo puhdistettiin uuttamalla asetonilla. 1940-luvun jälkeen yhdisteen syntetisoimiseksi yleistyi prosessi, jolla glykolihappoa valmistetaan korkeassa paineessa ja happamissa olosuhteissa formaldehydistä, hiilimonoksidista ja vedestä. Muita tapoja ovat oksaalihapon pelkistys, glykolin hapetus, glykolonitriilin hydrolyysi ja laboratoriomittakaavassa glykolaattiesterien hydrolyysi.[2][3][4]
Tärkein glykolinhapon yksittäinen käyttökohde on metallipintojen, syövytys, puhdistus ja kiillotus. Yhdisteen etuja ovat , että se on biohajoavaa eikä myrkyllistä. Lisäksi yhdistettä käytetään tekstiiliteollisuudessa nahan käsittelyyn, apuaineena tekstiilien värjäyksessä, raudan poistoon teollisuuden käyttämistä vesistä, biohajoavien polymeerien valmistuksessa ja lähtöaineena orgaanisen kemian synteeseissä.[2][3][4][5] Glykolihappoa käytetään myös kosmetiikassa ihovoiteissa ja kuorintavoiteissa. Glykolihappo tehoaa ryppyihin ja siloittaa niitä, mutta ihovoiteissa sen pitoisuus on liian pieni, jotta vaikutukset olisivat merkittäviä.[6]
Lähteet
- Glycolic acid – Substance summary PubChem. NCBI. Viitattu 13.7.2014.
- Alén, Raimo: Kokoelma orgaanisia yhdisteitä: Ominaisuudet ja käyttökohteet, s. 453. Helsinki: Consalen Consulting, 2009. ISBN 978-952-92-5627-3.
- Rathin Datta: Hydroxycarboxylic Acids, Kirk-Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, New York, 2004. Viitattu 13.7.2014
- Karlheinz Miltenberger: Hydroxycarboxylic Acids, Aliphatic, Ullmann's Encyclopedia of Industrial Chemistry, John Wiley & Sons, New York, 2000. Viitattu 13.7.2014
- George W. A. Milne: Gardner's commercially important chemicals, s. 310. John Wiley and Sons, 2005. ISBN 978-0-471-73518-2. Kirja Googlen teoshaussa (viitattu 13.7.2014). (englanniksi)
- Ryppysodassa siliää vain lompakko Tiede. 3.9.2007. Viitattu 13.7.2014.