Difluorikarbeeni
Difluorikarbeeni (CF2) on karbeeneihin kuuluva yhdiste. Muiden karbeenien tavoin se on erittäin reaktiivinen yhdiste ja esiintyy lähinnä välituotteena.
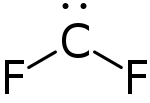
Suurimmilla osilla karbeeneista on alimman energian omaavalla perustilassaan triplettitilaisena. Fluoriatomit kuitenkin stabiloivat singlettitilan luovuttamalla elektroniparin tyhjälle d-orbitaalille. Perustilan ja ensimmäisen triplettitilan välinen energiaero on 56,6 kcal/mol. Elektroniparien luovuttamisen vuoksi difluorikarbeeni on vain kohtalaisen voimakas elektrofiili, useimmat karbeeneista ovat elektrofiileina voimakkaampia. Täten difluorikarbeeni on huomattavasti stabiilimpi kuin muut halogeeniatomin sisältävät karbeenit.[1][2][3]
Difluorikarbeenin valmistamiseen on useita eri tapoja. Näitä ovat esimerkiksi difluorikloorimetaanin dehydrohalogenointi käyttäen emäksenä alkoksideja tai alkyylilitiumyhdisteitä, fluorattujen orgaanisten yhdisteiden, kuten heksafluoripropyleenioksidin, perfluorisyklopropaanin, tetrafluorieteenin ja natriumklooridifluoriasetaatin, termolyysillä sekä elohopean, tinan, kadmiumin, piin ja fosforin organometalliyhdisteistä.[2][3]
Difluorikarbeenia käytetään pääasiassa alkeenien syklopropanointiin. Hyvin elektronirikkaat ja siten nukleofiiliset alkeenit reagoivat helposti difluorikarbeenin kanssa muodostaen difluorisyklopropaanirakenteen. Vähemmän nukleofiiliset alkeenit reagoivat sen kanssa kuitenkin vasta korotetussa lämpötilassa. Yhdiste reagoi myös imiinien kanssa muodostaen atsiridiinin johdannaisia.[2][3]
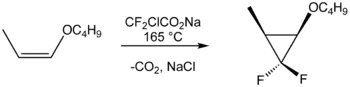
Lähteet
- Eric V. Anslyn, Dennis A. Dougherty: Modern physical organic chemistry, s. 59. University Science Books, 2006. ISBN 978-1-891389-31-3. Kirja Googlen teoshaussa (viitattu 04.01.2012). (englanniksi)
- Peer Kirsch: Modern Fluoroorganic Chemistry, s. 135. John Wiley & Sons, 2006. ISBN 978-3-527-60419-7. Kirja Googlen teoshaussa (viitattu 04.01.2012). (englanniksi)
- Dana Lyn S. Brahms & William P. Dailey: Fluorinated carbenes. Chemical reviews, 1996, 96. vsk, nro 5, s. 1585-1632.