Surfaktante
Surfaktanteak (tensoaktibo edo tensioaktiboak ere deituak) gainazal-tentsioaren bidez bi faseen arteko interfazean eragiten duten substantziak dira (adibidez, elkarren artean disolbaezinak diren bi likido). Surfaktante terminoa anglizismo bat da, surfactant hitzetik hartutakoa, zeina, halaber, Surface active agent (azaleko agente aktibo) hitzetik datorren terminoa den[1]. Etxeko teknologian erabiltzen direnean, emultsionatzaile deitzen zaie, hau da, emultsio bat lortu edo mantentzea ahalbidetzen duten substantziak. Uretan duten sakabanaketa handiagoa edo txikiagoaren eta mizelen edo koloideen egonkortze handiagoa edo txikiagoaren arabera, tensioaktiboak emultsionatzaile, hezegarri, garbigarri edo disolbatzaile gisa erabiltzen dira.


Surfaktanteak prozesu baten barruan ezpurutasun kopurua murrizteko eta horrela produktuari kalitate handiagoa eskaintzeko ere erabiltzen dira.
Surfaktanteen artean, arropa garbiketan aldizka erabiltzen diren substantzia sintetikoak daude, besteak beste, arropa garbigarriak, ontzi-garbigailuak, gainazaleko hautsa kentzekoak, dutxa-gelak eta xanpuak. XX. mendearen lehen erdian garatu ziren, eta, neurri handi batean, xaboi tradizionala ordezkatu dute. Gaur egun, erauzi bidez iturri naturaletatik ere ekoizten dira surfaktanteak, eta horietako batzuk oso onartuak dira kosmetika natural eta organikoan (poliglukosidoak).
Surfaktanteen sailkapena
Bere egitura molekularraren arabera
Surfaktanteen propietateak beren egitura molekularraren bidez lortzen dira. Surfaktanteak zati hidrofobo edo hidrofugo batez eta zati hidrofilo edo ur disolbagarri batez osatuta daude. Molekula anfifiloak omen dira.
| Surfaktanteak | Talde hidrofilikoa/k |  </img> </img> |
|---|---|---|
| tensioaktibo ez-ionikoa | –OH ( Alkohol anitzak), –O– ( Ether ) edo –O–CH 2 –CH 2 –OH konbinazioa (adibidez , gantz-alkohol etoxilatua ) | |
| tensioaktibo anionikoa | –COO − ( Karboxilatoa ), –SO 3 − ( Sulfonatoa ) edo –OSO 3 − ( Sulfatoa ) | |
| tensioaktibo katioikoa | R 4 N + ( Amina kuaternarioa ) | |
| surfaktante anfoteroa | batez ere –COO− ( karboxilatoa ) eta R 4 N + (amina kuaternarioa ) | |
Urarekin kontaktuan jartzean, banakako molekulak honela orientatzen dira: zati hidrofoboa ur-mailaren gainetik irtengo da, aireari begira, zati hidrofiloa urpean geratzen den bitartean. Beste fenomeno bat da molekula anfifiloak lerrokatzen direla: alde batean zati hidrofiloak eta bestean zati hidrofobikoak eta, beraz, burbuilak sortzen hasten direla; zati hidrofobikoak erdian gelditzen dira, eta ur disolbagarrien aztarnak uretan disolbaturiko periferian geratzen dira. Egitura horiei mizela deitzen zaie.
Sailkapena surfaktanteak elektrolito baten aurrean duen disoziazio ahalmenean eta bere propietate fisiko-kimikoan oinarritzen da. Horiek izan daitezke: ionikoak edo ez-ionikoak; eta, ionikoen barruan, azaleko jarduera aurkezten duen zatiak, duen kargaren arabera, hauek izango dira: anionikoak, kationikoak eta anfoteroak .
Azido ionikoek, urarekiko afinitate handia dutenek, ur-dipoloekiko duten erakarpen elektrostatikoak bultzatuta, kate hidrokarburoen disoluzioak haiekin arrasta ditzakete, adibidez, azido palmikoa, ia ionizaezina dena eta disolbaezina dena, sodio palmitatoa guztiz ionizatuta disolbagarria den bitartean.
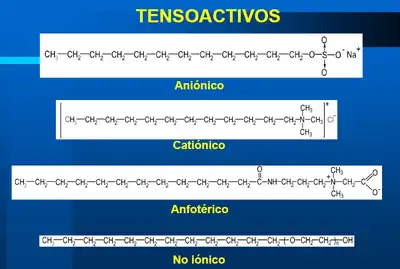
Tensioaktibo anionikoak
Surfaktante edo tensioaktibo guztien artean, anionikoak dira industria mailan gehien ekoizten direnak, bolumen aldetik. Eraginkortasun/prezio erlazioari dagokionez, orokorrean onenak dira[2].
Definizioz, surfaktante molekularen zati hidrofiloak karga negatiboa du. Hau karboxilato, sulfato, sulfonato edo fosfato talde bat izan ohi da.
Tensioaktibo kationikoak
Definizioz, surfaktante horien zati hidrofiloak karga positiboa du. Surfaktante horiek, normalean, atxikimendu handia dute substratu desberdinekiko, eta itsasgarritasun handia dute atxikimendu horretan. Konposatu horiek ezaugarritzen dituen datu esperimental bat da gainazaleko propietateak aldatzen dituztela eta gainazal hidrofilo bat hidrofobo bihurtzen dutela eta alderantziz[2].
Kate luzeko aminek eta haien gatzak, amina kuaternarioak zein imidazolineak, propietate bakterizidak dituzte, eta mikroorganismo desberdinak hil ditzakete, edo, gutxienez, hazkuntza atzeratu dezakete.
Surfaktante ez-ionikoak
Definizioz, surfaktante ez-ionikoak talde funtzional disoziagarriak (ionizagarriak) ez dituzten eta, beraz, uretan ioietan disoziatzen ez diren surfaktanteak dira. Surfaktante guztiak bezala, zati ez polar batez eta zati polar batez osatuta dago. Zati ez polarra denez, batez ere kate alifatikoa da (C12-C18 artean), nahiz eta tensioaktibo ez-ioniko ez-alifatikoak dauden. Talde polarrak alkohola edo eter taldea izan ohi dira[2].
Surfaktante anfoteroak
Definizioz, talde kationikoa eta talde anionikoa duten surfaktanteak dira. Anfotero terminoaren erabilerak murriztaileagoa egiten du: molekularen karga pH-arekin aldatu behar du, egitura zwitterionikoa duen pH bati erakutsiz, non molekulak ez duen kargarik, hau da, neutroa den (puntu isoelektrikoa)[2].
Erreferentzia
- Rosen MJ and Kunjappu JT (2012). Surfactants and Interfacial Phenomena (4th edición). Hoboken, New Jersey: John Wiley & Sons. p. 1. ISBN 1-118-22902-9
- Oldenhove de Guertechin, Louis. Handbook of Detergents, Part A: Properties (Serie: Surfactant Science). Capítulo 2: Surfactants: Classification. CRC Press. ISBN 978-0824714178