| Etenilfurano | |||
| Kemia formulo | |||
 | |||
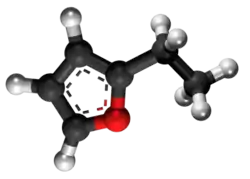
Etenilfurano | |||
 | |||
 | |||
| Vinilfurano ĉeestas en la rostita kafo. | |||
| Alternativa(j) nomo(j) | |||
| |||
| CAS-numero-kodo | 1487-18-9 31093-57-9 | ||
| ChemSpider kodo | 66515 | ||
| PubChem-kodo | 73881 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora aŭ flava likvaĵo | ||
| Molmaso | 94,11304 g mol−1 | ||
| Denseco | 0,944 g/cm−3[1] | ||
| Fandpunkto | -94°C [2] | ||
| Bolpunkto | 100,3°C [3] | ||
| Refrakta indico | 1,4992 | ||
| Ekflama temperaturo | 5,5°C[1] | ||
| Solvebleco | Akvo:nesolvebla[4] Solvebla en pentano, heksanoj, eteroj, tetrahidrofurano, etila acetato, metilena klorido kaj etanolo. | ||
| Mortiga dozo (LD50) | 57 mg/kg (buŝe) | ||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H225, H302+312+332, H302, H312, H332 | ||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P261, P264, P270, P271, P280, P301+317, P302+352, P303+361+353, P304+340, P317, P321, P330, P362+364, P370+378, P403+235, P501 | ||
(25 °C kaj 100 kPa) | |||
Vinilfurano aŭ etenilfurano estas organika kombinaĵo rezultanta per reduktado de 2-furanetanolo. Ĝi estas senkolora aŭ flava likvaĵo, nesolvebla en akvo sed solvebla en nepolaraj organikaj solvantoj. Vinilfurano posedas 6 karbonatomojn, 6 hidrogenatomojn kaj 1 oksigenatomon.
2-Vinilfurano, ankaŭ konata kiel 2-etenilfurano, estas organika kombinaĵo apartenanta al la familio de la ciklaj nesaturitaj hidrokarbonidoj. Ĝi estas senkolora ĝis palflava likvaĵo kun dolĉa, frukta odoro. 2-Vinilfurano, estas vaste uzata en diversaj sciencaj esploraj aplikoj pro siaj unikaj kemiaj proprecoj.
2-Vinilfurano, estis vaste uzata en diversaj sciencaj esplor-aplikoj. Ĝi estas uzata kiel komenca materialo por la sintezo de diversaj organikaj kombinaĵoj, inkluzive de farmaciaĵoj, agrokemiaĵoj kaj aromataĵoj. 2-Vinilfurano, ankaŭ estas uzata kiel gustiga agento en manĝaĵoj kaj trinkaĵoj.
2-Vinilfurano, havas unikan mekanismon de ago. Ĝi funkcias kiel Mikaelo-ricevanto, kio signifas, ke ĝi povas reakcii kun nukleofiloj kiel tioloj, aminoj kaj karboksilataj cidoj. Tiu reakcio kaŭzas la formadon de kovalentaj ligoj inter 2-Vinilfurano, kaj la nukleofilo, rezultigante la modifon de la proprecoj de la nukleofilo.
2-Vinilfurano, pruviĝis havi diversajn biokemiajn kaj fiziologiajn efikojn. Oni raportis, ke ĝi havas kontraŭinflamajn, antioksidajn kaj kontraŭkancerajn proprecojn. 2-Vinilfurano, ankaŭ pruviĝis malhelpi la kreskon de diversaj mikroorganismoj, inkluzive de bakterioj kaj fungoj.
2-Vinilfurano, havas plurajn avantaĝojn por laboratorio-eksperimentoj. Ĝi estas facile havebla kaj relative facile sintezebla. 2-Vinilfurano, ankaŭ estas stabila sub normalaj laboratoriokondiĉoj. Tamen, 2-Vinilfurano, havas kelkajn limigojn. Ĝi estas tre reakciema kaj povas reakcii kun diversaj nukleofiloj, igante ĝin malfacile kontroli ĝiajn reakciojn. 2-Vinilfurano, ankaŭ estas venena kaj povas kaŭzi haŭtan kaj okulan iriton.[5]
Sintezoj
Sintezo 1
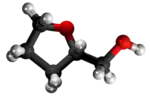
- Preparado de la vinilfurano per oksidado de la tetrahidrofurfurila alkoholo:
|
|
Sintezo 2
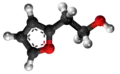
- Preparado de la vinilfurano per oksidado de 2-furanetanolo:
|
|
Sintezo 3
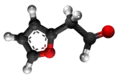
- Preparado de la vinilfurano per oksidado de 2-furanacetaldehido:
|
|
Sintezo 4
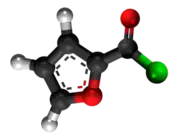
- Preparado de la etileno per traktado de furanila klorido kaj etileno:
|
|
Sintezo 5
- Preparado de la vinila klorido per traktado de furano kaj vinila klorido:
|
|
Sintezo 6
- Preparado per kataliza oksidado de la etilfurano:
|
|
Sintezo 7
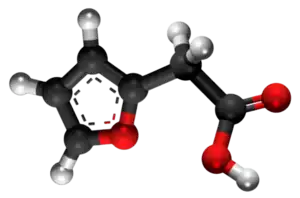
- Preparado de la vinilfurano per reduktado de furanoacetata acido:
|
|
Sintezo 8
- Preparado de la vinilfurano per reduktado de furanacetaldehido:
|
|