| S-tiolaktata acido | |||
 | |||
| Plata kemia strukturo de la 2-hidrokso-merkapto-propanoata acido | |||
 | |||
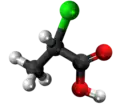
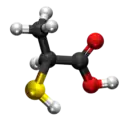
| Tridimensia strukturo de la Tiolaktata acido | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 79-42-5 | ||
| ChemSpider kodo | 56121 | ||
| PubChem-kodo | 62326 | ||
| Merck Index | 15,9493 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora aŭ flaveca oleeca substanco kun malagrabla odoro | ||
| Molmaso | 106.14 g·mol−1 | ||
| Denseco | 1.193 g cm−3 | ||
| Fandpunkto | 10 °C | ||
| Bolpunkto | 208 °C | ||
| Refrakta indico | 1,4809 | ||
| Ekflama temperaturo | 87 °C[1] | ||
| Acideco (pKa) | 3.74 | ||
| Solvebleco | Akvo:Solvebla en akvo, etanolo kaj acetono. | ||
| Mortiga dozo (LD50) | 730 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Risko | R22 R34 | ||
| Sekureco | S26 S36/37/39 S45 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj[2] | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H301, H311, H314, H330 | ||
| GHS Deklaroj pri antaŭgardoj | P260, P264, P270, P271, P280, P284, P301+310, P301+330+331, P302+352, P303+361+353, P304+340, P305+351+338, P310, P312, P320, P321, P330, P361, P363, P403+233, P405, P501 | ||
(25 °C kaj 100 kPa) | |||
Tiolaktata acido estas organika kombinaĵo derivata el la laktata acido kie la hidroksilo (-OH) estas anstataŭata de hidrogena-sulfido grupo (-SH). Ĝi estas senkolora oleeca substanco, solvebla en akvo kun malagrabla odoro. Ĝi estigas salojn per diversaj metaloj kaj uzatas en senharigaĵoj kaj preparaĵoj por konstantaj frizoj.
Sintezo
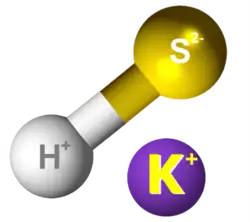
- En 1864, A. von Grote kaj Bernhard Tollens (1841-1918) preparis 2-merkaptolaktatan acidon per interagado de la 2-kloro-propanata acido kaj kalia hidrogeno sulfido aŭ kalia bisulfido:
|
|
- Preparado de la 2-tiolaktata acido per traktado de 2-kloropropanata acido kaj sulfida acido:
|
|
Literaturo
- Chemical Book
- Handbook of Preservatives, Michael Ash
- Fenaroli's Handbook of Flavor Ingredients, Fifth Edition, George A. Burdock
- Bulletin of the Chemical Society, Volume 34
Vidu ankaŭ
- Laktata acido
- Tioacetata acido
- Tioglikolata acido
- Akrilonitrilo
- Tiolaktatoj
- Levulinata acido
Referencoj
- ↑ Chemyq. Arkivita el la originalo je 2012-03-22. Alirita 2017-05-03.
- ↑ PubChem
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.