| Tiazolo | ||||
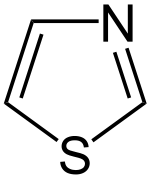 | ||||
| Plata kemia strukturo de la Tiazolo | ||||
 | ||||
| Tridimensia strukturo de la Tiazolo | ||||
| Alternativa(j) nomo(j) | ||||
| ||||
| Kemia formulo | ||||
| CAS-numero-kodo | 288-47-1 | |||
| ChemSpider kodo | 8899 | |||
| PubChem-kodo | 9256 | |||
| Merck Index | 15,9459 | |||
| Fizikaj proprecoj | ||||
| Aspekto | senkolora aŭ palflava likvaĵo kun malagrabla piridinsimila odoro | |||
| Molmaso | 85,12 g·mol−1 | |||
| Denseco | 1.2 g cm−3 | |||
| Fandpunkto | 116 °C | |||
| Bolpunkto | malkomponiĝas | |||
| Refrakta indico |
| |||
| Ekflama temperaturo | 26 °C | |||
| Acideco (pKa) | 2.5 | |||
| Solvebleco | Akvo:Malmulte solvebla en akvo | |||
| Mortiga dozo (LD50) | 983 mg/kg (buŝe) | |||
| Sekurecaj Indikoj | ||||
| Risko | R10 R22 R36/37/38 | |||
| Sekureco | S26 S36/37 | |||
| Pridanĝeraj indikoj | ||||
| Danĝero
| ||||
| GHS etikedigo de kemiaĵoj[1] | ||||
| GHS Damaĝo-piktogramo |
| |||
| GHS Signalvorto | Damaĝo | |||
| GHS Deklaroj pri damaĝoj | H225, H226, H302, H315, H318, H335 | |||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P261, P264, P270, P271, P280, P301+312, P302+352, P303+361+353, P304+340, P305+351+338, P310, P312, P321, P330, P332+313, P362, P370+378, P403+233, P403+235, P405, P501 | |||
(25 °C kaj 100 kPa) | ||||
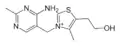
Tiazolo estas organika heterocikla kombinaĵo kiu enhavas sulfuron kaj nitrogenon. Ĝi estas la baza strukturo kaj rilatas al granda familio da derivaĵoj. Ĝi estas palflava likvaĵo kun piridinosimila odoro kaj ĝia ringo estas komponanto de pluraj naturproduktoj inter ili Vitamino B1.
| Familio de la Tiofeno | ||||||||
 |  |  |  | |||||
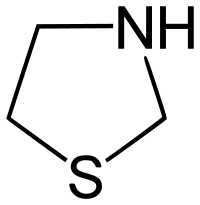
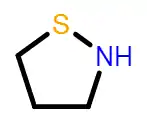
| Izotiazolo | ||||||||
 |  |  |  | |||||
Karakterizaĵoj
Tiazoloj estas membroj de la azolaj familio, heterociklaj kombinaĵoj kiuj inkluzivas la imidazolojn kaj oksazolojn. Tiazolo ankaŭ povas konsideriĝi kiel funkcia grupo. Oksazoloj estas komponaĵoj kunrilataj kie la sulfuro anstataŭis la oksigenon. Tiazoloj estas strukture similaj al imidazoloj, kie la sulfuro de la tiazolo estis anstataŭita de nitrogeno. Tiazolaj ringoj estas plataj kaj aromataj strukturoj.
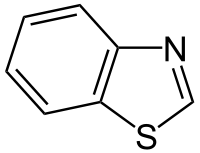
Tiazoloj troviĝas en varieco da specialigitaj produktoj, ofte fanditaj kun benzenaj derivaĵoj, la tiam konataj benzotiazoloj. Krom la Vitamino B1, la tiazola ringo troviĝas en la epotilono. Aliaj gravaj tiazolaj derivaĵoj estas la benzotiazoloj, ekzemple la kemia luciferino de la lampiro. Kvankam tiazoloj estas bone reprezentataj en biomolekuloj, la oksazoloj ne. Ĝi estas nature trovata en peptidoj kaj uzata en la disvolvo de peptidomimetikoj, aŭ molekuloj kiu imitas la funkcion kaj strukturon de la peptidoj.
Komercaj signifoplenaj tiazoloj inkludas ĉefe tinkturojn kaj fungicidojn. Trifluzamido', triciklazolo kaj tiabendazolo estas komercitaj por kontrolo de pluraj agrikulturaj pestoj. Alia vaste uzata tiazola derivaĵo estas la ne-steroida antiinflama drogo konata kiel Meliksicamo.
Sintezoj
Sintezo 1
- Tiazola sintezo de Hantzsch (1887) from izotiocianatoj:[2] Interagado de haloketonoj kaj tioamidoj estigas tiazolajn derivaĵojn, ezemple: 2,4-dumetil-tiazolo sintezeblas ekde la acetamido kun fosfora kvinsulfido kaj kloroacetono:

Sintezo 2
- Sintezo de Robert Robinson (1886-1975) kaj Siegmund Gabriel (1851-1924)[3], kiuj priskribis ĝin en 1909 kaj 1910 respektive[4][5] La reakcio okazas inter 2-acilamino-ketonoj en acida medio en ĉeesto de fosfora kvinsulfido:

Sintezo 3
- Sintezo de Ian Morris Heilbron (1886-1959) kaj Alan Hugh Cook (1922-2004). Estas reakcio inter α-aminonitriloj kaj karbona dusilfido por estigi la 5-amino-2-merkapto-tiazolojn.
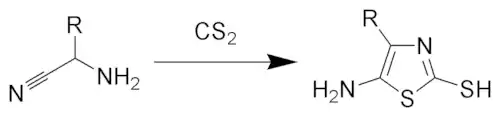
Sintezo 4
- Reakcio de Richard Herz (1867-1936): Estas kemia konvertigo de anilina derivaĵo al salo de Hertz kun dusulfura klorido sekvata per hidrolizo de la salo de Herz al la koresponda natria tiolato:

Literaturo
Kunrilataj kemiaĵoj
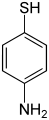
Aminotiofenolo 
Tiaduazoloj 

Klometiazolo 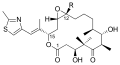
Epotilono 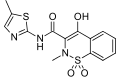
Meloksikamo 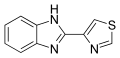
Tiabendazolo 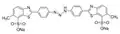
Flava tiazolo 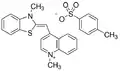
Oranĝa tiazolo 
Sulfatiazolo 
Abafungino 
Tifluzamido 
Triciklazolo 
Tiabendazolo
Vidu ankaŭ
- Heterociklaj kombinaĵoj
- Imidazolo
- Izotiazolo
- Morfolino
- Tiomorfolino
- Oksazolo
- Piperidino
- Piridino
- Pirimidino
- Pirolo
- Pirolidino
- Pirolino
- Tioamido
- Tiamino
- Tiazolino
- Tioformamido
- Arthur Hantzsch (1857-1935)
- Ian Morris Heilbron (1886-1959)
- Richard Herz (1867-1936)
- Robert Robinson (1886-1975)
- Siegmund Gabriel (1851-1924)
Referencoj
- ↑ PubChem
- ↑ Chemical Drug Design, Girish Kumar Gupta, Vinod Kumar
- ↑ Organic Chemistry Portal
- ↑ SynArchive.com
- ↑ Comprehensive Organic Synthesis



