| Sorbata acido | |||
 | |||
| Plata kemia strukturo de la Sorbata acido | |||
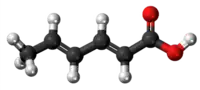 | |||
| Tridimensia kemia strukturo de la Sorbata acido | |||
 | |||
| Sorbata acido estis unue ekstraktita en 1859 ekde la sorpo far August von Hofmann (1818-1892) | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 110-44-1 | ||
| ChemSpider kodo | 558605 | ||
| PubChem-kodo | 643460 | ||
| Merck Index | 15,8847 | ||
| Fizikaj proprecoj | |||
| Aspekto | blanka kristala pulvoro | ||
| Molmaso | 112.128 g·mol−1 | ||
| Denseco | 1.205g cm−3 | ||
| Fandpunkto | 134.5 °C | ||
| Bolpunkto | 228 °C[1] | ||
| Ekflama temperaturo | 127 °C | ||
| Acideco (pKa) | 4.76 | ||
| Solvebleco | Akvo:1.6 g/L | ||
| Mortiga dozo (LD50) | 7360 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Riskoj | R36/37/38 | ||
| Sekureco | S24 S25 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H315, H319, H335[2] | ||
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405, P501 | ||
(25 °C kaj 100 kPa) | |||
Sorbata acido estas nesaturita organika acido ankaŭ konata kiel 2,4-heksanoduoata acido, konsistanta je blankaj nadloformataj kristaloj kun karakteriza odoro kaj uzata kiel nutro-konservanto. Ĝi estis unu ekstrakciita el la Sorbus aucuparia kaj el tiu planto venas ĝia nomo. Kiam longatempe ekspoziciita en aero, ĝi facile oksidiĝas kaj koloriĝas.
Ĝi estas nesolvebla en akvo sed miksebla kun glacia acetata acido (11,5%), etanolo (0,29%), duoksano (11%), acetono (9,2%) kaj izopropanolo (8,4%). Ĉi-netoksa kaj efika nutro-konservanto partoprenas en la normala metabola funkcio, povas oksidiĝi en akvo kaj karbona duoksido, kaj ne akumuliĝas en la homa korpo. Ĝia tokseco estas duono ol ĝia salo kaj 40-fojojn malpli ol la natria benzoato. Ĝi havas antioksidigajn kaj antimikrobajn proprecojn kaj uzatas en trink-fabrikado por preventi kontraŭ ŝimo, gisto kaj fungoj.
Historio
Sorbata acido estis unu priskribiita en 1859 de August von Hofmann (1818-1892) per hidrolizo de la distilitoleo de malmatura sorpo.[3] En 1900, Doebner unue sintezis ĝin per kondensiĝo de la krotonaldehido kaj malonata acido en piridina solvaĵo. La antimikrobaj kaj konservaj proprecoj de la sorbata acido estis unue malkovritaj, kaj en Usono, kaj en Germanio de E. Miller kaj C. M. Gooding en la fino de la jardeko 1930 kaj en la komenco de la jardeko 1940. En 1945 C. M. Gooding akiris la unuan usonan patenton.[4]
Sintezoj
Sintezo 1
Sorbata acido estiĝas per interagado de la ketenono kaj krotonaldehido en ĉeesto de boro-tri-fluorido:
2 |
Sintezo 2
Sorbata acido ankaŭ prepareblas per kondensiĝo de la malonata acido kaj krotonaldehido:
|
Literaturo
- Chemicalland21
- Handbook of Food Spoilage Yeasts, Tibor Deak, Larry R. Beuchat
- Introduction to Food Toxicology Takayuki Shibamoto,Leonard F. Bjeldanes
- Microbiological Safety and Quality of Food, Barbara Lund,Tony C. Baird-Parker, Grahame Warwick Gould
- Fisher's Contact Dermatitis, Robert L. Rietschel, Joseph F. Fowler, Alexander A. Fisher
- Handbook of Enology, The Microbiology of Wine and Vinifications, Pascal Ribéreau-Gayon, Denis Dubourdieu, B. Donèche, A. Lonvaud
Vidu ankaŭ
| ||||||
Referencoj
- ↑ Chemical Book
- ↑ Pubchem
- ↑ Food Additive Toxicology, Maga
- ↑ Antimicrobials in Food, Third Edition, P. Michael Davidson, John N. Sofos, A. Larry Branen




