| Pirazolo | |||||
 | |||||
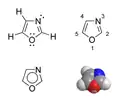
| Plata kemia strukturo de la Pirazolo | |||||
 | |||||
| Tridimensia strukturo de la Pirazolo | |||||
| Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | |||||
| CAS-numero-kodo | 288-13-1 | ||||
| ChemSpider kodo | 1019 | ||||
| PubChem-kodo | 1048 | ||||
| Merck Index | 15,8071 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | senkolora amargusta solido kun piridinodoro | ||||
| Molmaso | 68.08 g·mol-1 | ||||
| Denseco | 1.116 g cm−3 | ||||
| Fandpunkto | 69.5-70 °C | ||||
| Bolpunkto | 186-188 °C | ||||
| Solvebleco | Solvebla en akvo, etanolo kaj duetila etero | ||||
| Mortiga dozo (LD50) | 1010 mg/kg (buŝe) | ||||
| Sekurecaj Indikoj | |||||
| Risko | R22 R20/21/22 R36/37/38 R52 | ||||
| Sekureco | S26 S36/37 S37/39 S61 | ||||
| Pridanĝeraj indikoj | |||||
| Danĝero
| |||||
| GHS etikedigo de kemiaĵoj[1] | |||||
| GHS Damaĝo-piktogramo |
| ||||
| GHS Signalvorto | Damaĝo | ||||
| GHS Deklaroj pri damaĝoj | H302, H311, H314, H315, H318, H319, H335, H361, H371, H372, H412 | ||||
| GHS Deklaroj pri antaŭgardoj | P201, P202, P260, P261, P264, P270, P271, P273, P280, P281, P301+312, P301+330+331, P302+352, P303+361+353, P304+340, P305+351+338, P308+313, P309+311, P310, P312, P314, P321, P330, P332+313, P337+313, P361, P362, P363, P403+233, P405 | ||||
(25 °C kaj 100 kPa) | |||||
Pirazolo estas organika heterocikla kombinaĵo karakterizata per kvin-membra ringo je tri karbonatomoj kaj du apudaj nitrogenatomoj. Pirazoloj estas malforta bazo kun pKb egala al 11.5. Ĝi estas klaso da komponaĵoj enhavantan la pirazolan ringon kaj uzata en farmacio nature trovata aŭ artefarite sintezita.
Pirazoloj enhavas du duoblajn ligilojn en la molekulo, kiu donas aromatan karakteron al la substanco. Ili estas stabilaj komponaĵoj kaj povas ekzisti laŭ izomeraj strukturoj. Pirazoloj estas raraj en naturo kiam komparataj al la imidazoloj, kiuj estas vaste trovataj kaj posedas centran rolon en multaj biologiaj procezoj.
Historio
La nomo pirazolo estis donita al ĉi-klaso da komponaĵoj en 1883, far la germana kemiisto Ludwig Knorr (1859-1921). En klasika metodo kreita de la germana kemiisto Hans von Pechmann (1850-1902), la pirazolo estis sintezita ekde la acetileno kaj duazometano. En 1959, la unua natura pirazolo, tio estas la pirazolila alanino, estis izolita en semoj de akvomelonoj.
Sintezo
- En 1898, la germana kemiisto Hans von Pechmann (1850-1902) disvolvis la sintezon de la pirazolo interagante la acetilenon kun la duazometano:
- Ĝenerale, la pirazoloj sintezeblas laŭ reakcio de α,β-nesaturitaj aldehidoj kun la hidrazino, sekvata de posta senhidrogenigo:
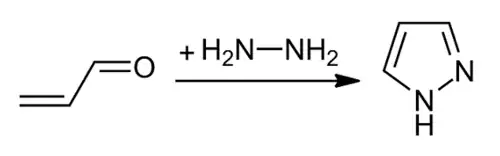
Reakcio
- Piroloj reakcias kun kalia borohidrido por estigi klason da ligantoj konataj kiel skorpionatoj. La pirazolo ĝustadire reakcias kun la kalia borohidrido sub alta temperaturo (200 °C) por formi la tridentatan liganton konatan kiel Tp liganton aŭ tripirazolan liganton.
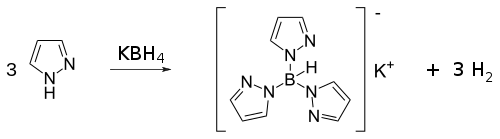
Proprecoj
En medicino, derivaĵoj el la pirazoloj uzatas pro ilia analgezia, anti-algesia, kontraŭ-inflama, kontraŭ-febra, kontraŭmisritma, trankviliga, muskolkvietiga, psikostimula, anti-konvulsia, kontraŭdiabeta, unuaminaoksidazo-inhiba, antifunga, kaj antibakteria proprecoj. La pirazolo estas konkurenca inhibanto de la enzimo alkohol-senhidrogenazo, respondeca pri la transformo de alkoholoj en aldehidoj.
Literaturo
Kunrilataj kemiaĵoj
Fenilbutazono 
Indazolo 


Triptofano 
Diazolo 
Metil-pirazolo pyrazole.png.webp)
Piridil-pirazolo 
Fenil-pirazolo 
Dumetil-pirazolo Triazolo(4%252C3-a)pyrazine.png.webp)
Triazolo-pirazino 
Amino-metil-pirazolo 
Pirazolila alanino
Vidu ankaŭ
- Hans von Pechmann (1850-1902)
- Ludwig Knorr (1859-1921)
- Pirolo
- Imidazolo
- Heterociklaj kombinaĵoj
- Triptofano




