| Nitro-anizolo | ||
 | ||
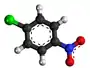
| Plata kemia strukturo de la p-nitro-anizolo | ||
 | ||
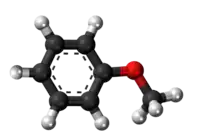
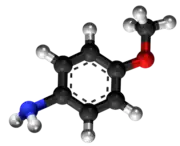
| Tridimensia kemia strukturo de la p-nitro-anizolo | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 100-17-4 | |
| ChemSpider kodo | 21106148 | |
| PubChem-kodo | 7485 | |
| Merck Index | 15,6671 | |
| Fizikaj proprecoj | ||
| Aspekto | verda aŭ bruna solidaĵo | |
| Molmaso | 153,137 g·mol-1 | |
| Denseco | 1,233g cm−3[1] | |
| Fandpunkto | 51°C | |
| Bolpunkto | 260°C | |
| Refrakta indico | 1,5030 | |
| Ekflama temperaturo | 127 °C | |
| Solvebleco | Akvo:0,468 g/L [2] | |
| Mortiga dozo (LD50) | 300 mg/kg (buŝe)[3] | |
| Sekurecaj Indikoj | ||
| Riskoj | R52/53 R68 | |
| Sekureco | S61 S36/37 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H341, H412 | |
| GHS Deklaroj pri antaŭgardoj | P201, P202, P273, P281, P308+313, P405, P501[4] | |
(25 °C kaj 100 kPa) | ||
Nitro-anizolo aŭ C7H7NO3 estas organika aromata komponaĵo, verda aŭ bruna solidaĵo apartenanta al la familio de la nitro-kombinaĵoj (-NO2) kaj anizolo, uzata en kemiaj sintezoj. Sennombraj nitroanizolaj derivaĵoj estas gravaj kiel reakciaĵoj, antaŭaĵoj de vasta gamo da substancoj uzataj en industrio, farmacio kaj agrikulturo.
Biologie, nitroanizoloj estas senmetiligitaj al nitrofenoloj de la homhepata mikrosomoj. Krom tio, nitroanizoloj fotokemie reakcias kun nukleofilaj aromataĵoj interŝanĝe de hidroksidaj jonoj por formi metoksofenolojn kaj p-nitrofenolojn.
Sintezoj
Sintezo 1
- Preparado per interagado de p-kloro-nitro-benzeno kaj natria metoksido:
|
|
Sintezo 2
- Preparado per traktado de nitrita acido sur anizolo:
|
|
Sintezo 3
- Preparado per traktado de nitrila klorido kaj anizolo:
|
|
Sintezo 4
- Preparado per traktado de nitrila fluorido kaj anizolo:
|
|
Sintezo 5
- Preparado per reakcio de anizila bromido kun kalia nitrato:
|
|
Sintezo 6
- Preparado per reakcio de anizila bromido kun kalia nitrato:
|
|
Reakcioj
Reakcio 1
- Preparado de anizidino en ĉeesto de amonia formiato kaj zinko:
|
|
Reakcio 2
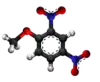
- Reakcio kun nitrita acido produktas 2,4-dunitroanizolon:Dunitroanizolo estas flava solidaĵo solvebla en etanolo kaj duetila etero. [5]
|
|
Reakcio 3
- Hidrolizo de la nitro-anizolo:
|
|
Reakcio 4
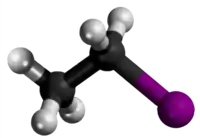
- Etiligo de la nitro-anizolo:
|
|
Reakcio 5
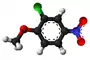
- Preparado de la kloro-nitro-anizolo (CAS-numero 4920-79-0):
|
|
Reakcio 6
- Preparado de la metila nitro-anizolo (CAS-numero 50741-92-9):
|
|
Reakcio 7
- Preparado de la fenila nitro-anizolo (CAS-numero 15854-75-8):
|
|
Literaturo
Referencoj
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.