| Natria tritionato | |||
 | |||
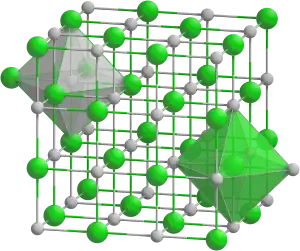
| Kemia strukturo de la Natria tritionato | |||
 | |||
| 3D Kemia strukturo de la Natria tritionato | |||
| Alternativa(j) nomo(j) | |||
| Natria salo de tritionata acido | |||
| Kemia formulo | |||
| CAS-numero-kodo | 21335-56-8 | ||
| ChemSpider kodo | 491 | ||
| Fizikaj proprecoj | |||
| Molmaso | 238,1739 g mol−1 | ||
| Sekurecaj Indikoj | |||
| Risko | R36 R37 R38 | ||
| Sekureco | S26 S36 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H315, H319, H335 | ||
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405, P501 | ||
(25 °C kaj 100 kPa) | |||
Natria tritionato, tritionato de natrio aŭ Na2S3O6 estas okso-salo de tritionata acido kaj natria hidroksido.[1] Solvaĵoj de natria tritionato en akva solvaĵo donas tritionatan acidon. Tritionata acido estas malkovrita de Langlois, en 1842.[2]
Sintezo
- Neŭtraliga reakcio inter tritionata acido kaj natria hidroksido:
- Natria tritionato prepareblas per oksidado de natria tiosulfato kaj hidrogena peroksido:[3]
- Natria tritionato ankaŭ prepareblas per pasado de sulfura duoksido tra solvaĵo de natria tiosulfato:[3][4]
- Preparado per interagado de natria bisulfito kaj unusulfura duklorido:[5]
- Tritionatoj prepareblas per traktado de natria tiosulfato kaj natria bisulfito ĉeeste de jodo en akva solvaĵo:
Reakcio
- Hidroliza reakcio de natria tritionato:
Literaturo
Vidu ankaŭ
| ||||||
Referencoj
- ↑ Concise Encyclopedia Chemistry, Mary Eagleson
- ↑ Digital Library of India
- 1 2 Advanced Inorganic Chemistry, Volume 1, Satya Prakash
- ↑ Preparation of Sodium trithionate
- ↑ The Chemistry of Lithium, Sodium, Potassium, Rubidium, Cesium and Francium ..., William A. Hart, O. F. Beumel, Thomas P. Whaley
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.