| Natria superoksido | |||
 | |||
| Kemia strukturo de la Natria superoksido | |||
 | |||
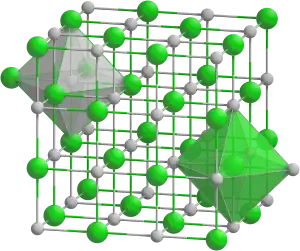
| 3D Kemia strukturo de la Natria superoksido | |||
 | |||
| Kristala strukturo de natria superoksido | |||
| Kemia formulo | |||
| CAS-numero-kodo | 12034-12-7 | ||
| ChemSpider kodo | 55460 | ||
| PubChem-kodo | 61542 | ||
| Fizikaj proprecoj | |||
| Aspekto | Flava aŭ oranĝokolora kristala solido | ||
| Molmaso | 54.9886 g mol−1 | ||
| Denseco | 2,2 g/cm3 | ||
| Fandopunkto | 551.7 °C (1,025.1 ℉; 824.9 K) | ||
| Bolpunkto | Malkomponiĝas | ||
| Solvebleco | Akvo:Malkomponiĝas | ||
| Ekflama temperaturo | Ne bruliva | ||
| Sekurecaj Indikoj | |||
| Risko | R35 | ||
| Sekureco | S(S1/2) S26 S37/39 S45 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H271, H290, H314 | ||
| GHS Deklaroj pri antaŭgardoj | P280, P301+330+331, P303+361+353, P305+351+338, P310 | ||
(25 °C kaj 100 kPa) | |||
Natria superoksido, superoksido de natrio aŭ NaO2 estas neorganika komponaĵo, flava aŭ oranĝokolora substanco, peraĵo en la oksidigo de natrio kaj oksigeno. Natria superoksido estas forta oksidigagento uzata en submarŝipoj laŭ la sama maniero kiel la natria peroksido, tamen, ĝi forte reakcias kun humideco kaj karbona duoksido.[1]
Sintezo
Sintezo 1
- Superoksido de natrio preparata per traktado de natria peroksido kaj oksigeno sub alta premo:
|
|
Sintezo 2
|
|
Reakcioj
Reakcio 1
- Ĝi malkomponiĝas sub altaj temperaturoj:
|
|
Reakcio 2
- Ĝi malkomponiĝas per interagado kun akvo:
|
|
Reakcio 3
- En la ĉeesto de katalizilo MnO2, la reakcio okazas laŭ la malsupra skemo:
|
|
Reakcio 4
- Natria superoksido reakcias kun klorida acido:
|
|
Reakcio 5
- Ĝi estas atakata de karbona duoksido:
|
|
Reakcio 6
- Kiam hejtata, ĝi reakcias kun karbona unuoksido:
|
|
Reakcio 7
- Natria superoksido estas forta oksidigagento:
|
|
Reakcio 8
- Kun aluminio ĝi estigas natrian aluminiaton:
|
|
Proprecoj
Natria superoksido estas paramagneta substanco tiel kiel oni povas atendi de anjono O2−. Ĝi facile hidrolizo|hidroliziĝas]] por estigi miksaĵon da natria hidroksido, oksigeno kaj hidrogena peroksido. En meditemperaturo, ĝia strukturo estas kuba malordigita strukturo kun faco centrita. Tiaj studoj estis faritaj de Templeton kaj Dauben kiuj venis al la konkludo ke la natria superoksido havas malordigitan strukturon de la pirito.[2]
Literaturo
- Nature
- Cornell University Library
- Cameo Chemicals
- ACS Publishing
- Chemical Book
- Superoxide Ion Chemistry and Biological Implications, Volume 1, Igor B. Afanas'ev
- Sasol Encyclopaedia of Science and Technology, G.C. Gerrans, P. Hartmann-Petersen, Rasmus Hartmann-Petersen
| ||||||
Referencoj
- ↑ Sodium, Anne O'Daly
- ↑ Progress in Inorganic Chemistry, Volume 4. F. Albert Cotton