| Natria perklorato | ||||
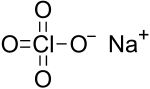 | ||||
| Kemia strukturo de la Natria perklorato | ||||
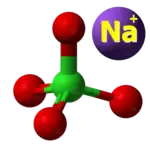 | ||||
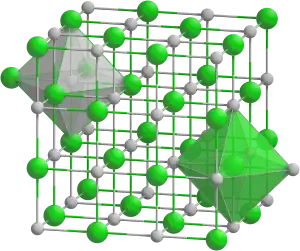
| Tridimensia strukturo de la natria perklorato | ||||
| Kemia formulo | ||||
| CAS-numero-kodo | ||||
| ChemSpider kodo | 22668 | |||
| PubChem-kodo | 522606 | |||
| Fizikaj proprecoj | ||||
| Aspekto | Blanka kristala solido | |||
| Molmaso |
| |||
| Smiles | [Na+].[O-]Cl(=O)(=O)=O | |||
| Denseco |
| |||
| Refrakta indico | 1,4617 | |||
| Fandopunkto | 468 °C (874 ℉; 741 K) (malkomponiĝas, anhidra) 130 °C (unuhidrata) | |||
| Bolpunkto | 482 °C (900 ℉; 755 K) (malkomponiĝas, unuhidrata) | |||
| Ekflama temperaturo | 400 °C (752 ℉; 673 K) °C | |||
| Sekurecaj Indikoj | ||||
| Risko | R9 R22 R36 R48 | |||
| Sekureco | S2 S13 S22 S27 | |||
| Pridanĝeraj indikoj | ||||
| Danĝero
| ||||
| GHS etikedigo de kemiaĵoj | ||||
| GHS Damaĝo-piktogramo |
| |||
| GHS Signalvorto | Damaĝa substanco | |||
| GHS Deklaroj pri damaĝoj | H203, H271, H302, H319, H373, H411 | |||
| GHS Deklaroj pri antaŭgardoj | P220, P264, P270, P273, P305+351+338, P352 | |||
(25 °C kaj 100 kPa) | ||||
Natria perklorato, perklorato de natrio aŭ NaClO4 estas neorganika kombinaĵo de natrio kaj perklorata acido, blanka kristala substanco, higroskopa, kaj tre solvebla en akvo kaj alkoholo. Ĝi estas komerce trovebla kiel unuhidrata salo, kiu havas romban kristalan sistemon.
Uzoj
Natria perklorato estas antaŭilo al multaj perklorataj saloj, ofte pro ĝia alta solvebleco (209 g/100 mL ĉe 25 °C). Perklorata acido prepareblas per traktado de HCl kaj natria perklorato.
Natria perklorato preskaŭ ne uzatas en pirotekniko pro ĝia alta higroskopeco, anstataŭe amonia perklorato kaj kalia perklorato estas prefereblaj. Ĉi-salos preparatas per duobla malkompiĝo el solvaĵo de natria perklorato kaj kalia aŭ amonia kloridoj.
Perklorato de natrio havas sennombrajn uzojn en laboratorio, ofte kiel nereaktiva agento. Ekzemple: ĝi uzatas por norma DNA ekstraktado kaj hibridigaj reakcioj en molekulabiologio. En medicino, natria perklorato povas uziĝi por bloki jodokaptadon antaŭ administrigo de jodkontrastaj agentoj en pacientoj kun subklinika hipertiroidismo[1].
Sintezo
- Natria perklorato prepareblas per termo-disproporcio de la natria klorato:
Reakcioj
- Natria perklorato eksplode reakcias kun fruktozo estigante karbonan duoksidon:[2]
- Natria perklorato reakcias kun amonia klorido por estigi nitrogenon, natria klorido kaj klorida acido:[3][4]
- Sulfata acido atakas natrian perkloraton estigante perkloratan acidon:
YouTube
Literaturo
Referencoj
- ↑ Subklinika hipertiroidismo rilatas al malsano kiu ne estas sufiĉe serioza por prezenti difinitajn aŭ facile observeblajn simptomojn.
- ↑ Lecture Demonstrations
- ↑ WebQC
- ↑ Oocities
| ||||||