| Natria ftalato | ||
 | ||
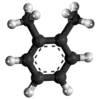
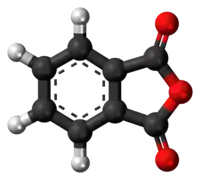
| Kemia strukturo de la Dunatria ftalato | ||
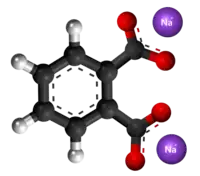 | ||
| Tridimensia kemia strukturo de la Natria ftalato | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 15968-01-1 | |
| ChemSpider kodo | 76850 | |
| PubChem-kodo | 85215 | |
| Fizikaj proprecoj | ||
| Molmaso | 210,094 g mol−1 | |
| Bolpunkto | 378.3 °C | |
| Solvebleco | Akvo:Solvebla | |
| Mortiga dozo (LD50) | 2,1 mg/kg (muso, buŝa) | |
| Ekflama temperaturo | 196.7 °C°C | |
| Sekurecaj Indikoj | ||
| GHS etikedigo de kemiaĵoj[1] | ||
| GHS Damaĝo-piktogramo |
| |
| GHS Signalvorto | Damaĝa substanco | |
| GHS Deklaroj pri damaĝoj | H335, H360 | |
| GHS Deklaroj pri antaŭgardoj | P201, P202, P281, P308+313, P405, P501 | |
(25 °C kaj 100 kPa) | ||
Natria ftalato, ftalato de natrio aŭ C8H4Na2O4 estas organika natria salo de ftalata acido, kiu povas ekzisti sub du formoj: ununatria kaj dunatria, ankaŭ konata kiel unubaza aŭ dubaza. Nuntempe, 80% de la monda produktado de ftalata acido por preparado de natria ftalato devenas el la aromata hidrokarbonido orto-ksileno. Ankaŭ eblas produkti ftalatan acidon el la naftaleno, procezo tre uzata en Japanio[2]. En la procezo ekde la ksilolo produktiĝas iom da maleata anhidrido.
Sintezo
- Natria ftalato estas sintezita ekde oksidigo de orto-ksilolo. La "ftalata anhidrido" produktita reakcias kun kaŭstika sodo rezultante en la natria ftalato:
|
|
- La supraj reakcioj povas esti reprezentataj laŭ la tri sekvaj etapoj:
- 1 - Oksidado de orto-ksilolo al ftalata acido
- 2 - Neŭtraliga reakcio inter ftalata acido kaj kaŭstika sodo:
Vidu ankaŭ
Literaturo
| ||||||
Referencoj
- ↑ PubChem
- ↑ Industrial Aromatic Chemistry: Raw Materials · Processes · Products, Heinz-Gerhard Franck, Jürgen W. Stadelhofer
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.