| Lizino | ||
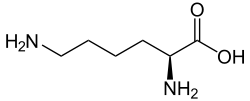 | ||
| Plata kemia strukturo de la Lizino | ||
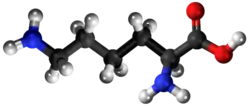 | ||
| Tridimensia kemia strukturo de la Lizino | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 70-54-2 | |
| ChemSpider kodo | 843 | |
| PubChem-kodo | 5962 | |
| Merck Index | 15,5697 | |
| Fizikaj proprecoj | ||
| Aspekto | blanka solidaĵo | |
| Molmaso | 146.19 g·mol−1 | |
| Denseco | 1.125g cm−3 | |
| Fandpunkto | 224.5 °C | |
| Acideco (pKa) | 2.18 | |
| Solvebleco | Akvo:1500 g/L | |
| Mortiga dozo (LD50) | 10000 mg/kg (buŝe) | |
| Sekurecaj Indikoj | ||
| Riskoj | R34 R36/37/38 | |
| Sekureco | S26 S36/37/39 S45 S24/25 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS etikedigo de kemiaĵoj | ||
| GHS Damaĝo-piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H315, H319, H335[1] | |
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405, P501 | |
(25 °C kaj 100 kPa) | ||
Lizino (2,6-diaminoheksanacido) (simbolo Lys aŭ K) apartenas al la 20 proteinogenaj (proteinformantaj) aminoacidoj, kiuj estas koditaj tra bazotriopo de RNA, por la uzo ĉe la proteina biosintezo en bazmateriala ŝanĝo de la organismoj.
Proprecoj
Ĝi apartenas kun arginino kaj histidino al la grupo de bazaj aminoacidoj aŭ heksonbazoj. Tiuj entenas bazan kemian grupon- ĉe lizino unu liberan aminogrupon en la flanka ĉeno-, pro kio ili regas kiel lesivoj. La ŝargo de lizino estas pH-dependa (pK-valoro: ~ 10).
Apero
Lizino apartenas al esencaj aminoacidoj por la homo, ĝin povas la homa organismo mem ne produkti kaj tiel ĝin devas akcepti kun nutrado. La plenkreska homo bezonas tage ĉirkaŭ 1–1,5 g da lizino. Tre multan lizinon entenas la fiŝo sed ankaŭ mungfaboj.
Referencoj
Eksteraj ligiloj
- http://www.chem.qmul.ac.uk/iubmb/enzyme/reaction/AminoAcid/Lys1.html
- http://www.chem.qmul.ac.uk/iubmb/enzyme/reaction/AminoAcid/Lys2.html
- http://www.chem.qmul.ac.uk/iubmb/enzyme/reaction/AminoAcid/Lys3.html
- http://www.compchemwiki.org/index.php?title=Lysine Arkivigite je 2008-04-29 per la retarkivo Wayback Machine
| ||||||
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.


