| Krotonaldehido | ||||||
 | ||||||
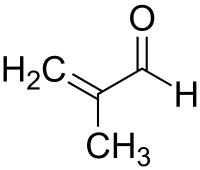
| Plata kemia strukturo de la Krotonaldehido | ||||||
-Crotonaldehyde_3D_ball.png.webp) | ||||||
| Tridimensia strukturo de la Krotonaldehido | ||||||
| Alternativa(j) nomo(j) | ||||||
| ||||||
| Kemia formulo | ||||||
| CAS-numero-kodo | ||||||
| ChemSpider kodo | 394562 | |||||
| PubChem-kodo | 447446 | |||||
| Merck Index | 15,2587 | |||||
| Fizikaj proprecoj | ||||||
| Aspekto | senkolora likvaĵo kun akra sufokiga odoro | |||||
| Molmaso | 70.09 g·mol−1 | |||||
| Denseco | 0.846 g cm−3 | |||||
| Fandpunkto | −76.5 °C | |||||
| Bolpunkto | 104 °C | |||||
| Refrakta indico | 1,4362 | |||||
| Ekflama temperaturo | 13 °C | |||||
| Memsparka temperaturo | 207 °C | |||||
| Solvebleco | Akvo:18.1 g/100 ml | |||||
| Mortiga dozo (LD50) | 80 mg/kg (buŝe) | |||||
| Sekurecaj Indikoj | ||||||
| Risko | R11 R24/25 R37/38 R41 R48/22 R50 R61 | |||||
| Sekureco | S26 S28 S36/37/38/ S45 S61 | |||||
| Pridanĝeraj indikoj | ||||||
| Danĝero
| ||||||
| GHS etikedigo de kemiaĵoj[1] | ||||||
| GHS Damaĝo-piktogramo |
| |||||
| GHS Signalvorto | Damaĝa substanco | |||||
| GHS Deklaroj pri damaĝoj | H225, H301, H311, H315, H330, H335, H341, H373, H400 | |||||
| GHS Deklaroj pri antaŭgardoj | P210, P280, P304+340, P310, P302+352 | |||||
(25 °C kaj 100 kPa) | ||||||
Krotonaldehido estas kemia komponaĵo, larmiga likvaĵo malmulte solvebla en akvo kaj miksebla en organikaj solvantoj. Kiel nesaturita aldehido, la krotonaldehido estas multeuza peranto en organikaj sintezoj, kiel surfaktanto, paperfabrikado, insekticido, ledotanado, ktp.. Ĝi nature okazas en pluraj nutraĵoj tia kia la sojoleo.
Krotonata aldehido eksplode reakcias kun oksidigiloj: reakcio kun nitrata acido rezultas en spontanea sparkigo. Kontakte kun fortaj acidoj kaj bazoj, la krotonaldehido spertas ekzoterman kondensiĝan reakcion. Reakcio kun la 1,3-butadueno estas aparte eksplodema.
Kvankam milde malpli toksa, la krotonaldehido kemie kaj toksologie similas al akroleino, kiu estas taksata kiel ekstreme toksa per inhalado kaj irita al okuloj. Tiel kiel la akroleino, ĝiaj vaporoj kaŭzas seriozajn kaj dolorajn okuliritojn, damaĝo al korneo, larmigado, irito de la nazalaj membranoj, pulminflamo (plenigo de pulmoj kun fluidaĵoj) kaj gastrointestaj damaĝoj kiam ingestita.
Sintezo
- Preparado de krotoanaldehido ekde la acetaldehido en ĉeesto de natria hidroksido sub milda temperaturo. La 3-hidrokso-butanalo estiĝas per aldola kondensiĝo. En dua etapo, ĝi reakcias kun acetata acido kun akvoforigo por doni krotonaldehidon:[2]

- Procezo de hidroformiligo de la miksaĵo konsistante je propileno, karbona unuoksido kaj hidrogeno.
- CH3-CH=CH2 + CO + H2 H3C-CH=CH2-CH-OH
Reakcio
- Krotonata acido estiĝas per oksidado de la krotonaldehido:

- Krotila alkoholo prepareblas per hidrogenigo de la krotonaldehido:

Literaturo
- Chemical Book
- Acute Exposure Guideline Levels for Selected Airborne Chemicals, Volume 6, National Research Council, Board on Environmental Studies and Toxicology, Committee on Toxicology, Committee on Acute Exposure Guideline Levels
- Hamilton and Hardy's Industrial Toxicology, Raymond D. Harbison, Marie M. Bourgeois, Giffe T. Johnson
- Proctor and Hughes' Chemical Hazards of the Workplace, Nick H. Proctor, James P. Hughes, Gloria J. Hathaway
- Handbook of Polymer Synthesis, Hans R. Kricheldorf
- Handbook of Commercial Catalysts: Heterogeneous Catalysts, Howard F. Rase
- Cysteine Endopeptidases: Advances in Research and Application: 2011 Edition
- Chemicalland21
Kunrilataj kemiaĵoj
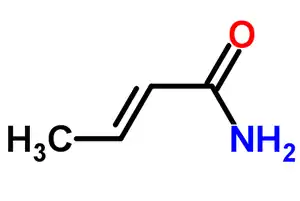
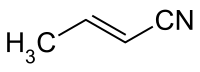
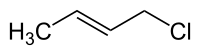
Krotila klorido 
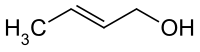
Vidu ankaŭ
Referencoj
- ↑ Αlfa Aesar
- 1 2 Industrial Organic Chemistry, Klaus Weissermel, Hans-Jürgen Arpe







