| Karbona disulfido | ||||
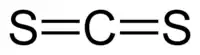 | ||||
| Plata kemia strukturo de la Karbona disulfido | ||||
 | ||||
| Tridimensia kemia strukturo de la Karbona disulfido | ||||
| Alternativa(j) nomo(j) | ||||
| ||||
| Kemia formulo | ||||
| CAS-numero-kodo | 75-15-0 | |||
| ChemSpider kodo | 6108 | |||
| PubChem-kodo | 6348 | |||
| Merck Index | 15,1811 | |||
| Fizikaj proprecoj | ||||
| Aspekto | senkolora toksa volatila brulema likvaĵo kun malagrabla odoro | |||
| Molmaso | 76131 g·mol−1 | |||
| Denseco | 1.2632g cm−3 | |||
| Fandpunkto | −111.6 °C[1] | |||
| Bolpunkto | 46.5 °C | |||
| Refrakta indico | 1,6319 | |||
| Ekflama temperaturo | −30 °C | |||
| Memsparka temperaturo | 95 °C | |||
| Solvebleco | Akvo:2.17 g/L | |||
| Mortiga dozo (LD50) | 1200 mg/kg (buŝe) | |||
| GHS etikedigo de kemiaĵoj | ||||
| GHS Damaĝo-piktogramo |
| |||
| GHS Signalvorto | Damaĝo | |||
| GHS Deklaroj pri damaĝoj | H225, H304, H315, H319, H361, H372, H373[2] | |||
| GHS Deklaroj pri antaŭgardoj | P201, P202, P210, P233, P240, P241, P242, P243, P260, P264, P270, P280, P281, P301+310, P302+352, P303+361+353, P305+351+338, P308+313, P314, P321, P331, P332+313, P337+313, P362, P370+378, P403+235, P405, P501 | |||
(25 °C kaj 100 kPa) | ||||
Karbona disulfido estas senkolora, toksa, volatila, brulema likvaĵo kun malagrabla odoro konsistanta je unu karbonatomo kaj du sulfuratomoj. Ĝi estas ne-polara solvanto kaj deirmaterialo por pluraj kemiaj sintezoj. Karbona disulfido estas danĝere brulema kaj ĝiaj ekflama kaj memsparka temperaturoj estas rimarkinde malaltaj.
Vaporoj de karbona disulfido estigas eksplodajn miksaĵojn en la aero kaj ĝiaj miksaĵoj kun fluoro aŭ kloro estas brulemaj ĉe mediaj temperaturoj. Grandaj kvantoj da karbona disulfido uzatas en la manufakturo de la rajona fibro, celofano kaj karbona tetraklorido.
Pli etaj kvantoj uzatas en procezoj je solvanto-ekstraktado aŭ konvertiĝas en aliaj kemiaĵoj, ĉefe kiel akceliloj en la kaŭĉuko-vulkanizado kaj agentoj uzataj en floto-procezoj por erco-koncentrigo. Karbona disulfido estas solvebla en etanolo, benzeno, kloroformo kaj karbona tetraklorido. Ĝi estas neakordigebla kun fortaj oksidigagentoj, azidoj, aluminio kaj zinko.
Sintezoj
Sintezo 1
| C + 2S → CS2 |
Sintezo 2
| 2 CH4 + S8 → 2 CS2 + 4 H2S |
Reakcioj
Reakcio 1
- Natria tiokarbonato preparatas per agado de karbona diulfido kaj natria bisulfido:
Reakcio 2
- Natria tiokarbonato same prepareblas per traktado de karbona disulfido kaj natria hidroksido:
Reakcio 3
- Natria duetila-dutiokarbamato estiĝas per traktado de karbona disulfido kun duetilamino en la ĉeesto de natria hidroksido:
Reakcio 4
- Karbona disulfido reakcias kun kloro en ĉeesto de katalizilo por estigi karbonan kvarkloridon:
| CS2 + 3 Cl2 |
Reakcio 5
- Traktado de amonia bisulfido kaj karbona disulfido estigas amonian tiokarbonaton:
Reakcio 6
- Amonia tiokarbonato estiĝas per traktado de amonia kvinsulfido kaj karbona disulfido:
Reakcio 7
- Tioureo estiĝas per traktado de la amoniako kun karbona disulfido:
Reakcio 8
- Duetilamino reakcias kun karbona disulfido en alkala medio donante duetil-dutiokarbamatojn:
| (C2H5)2NH + CS2 + KOH → (C2H5)2NC(S)SK + H2O
|
Reakcio 9
- Trietilamino reakcias kun karbona disulfido en alkala medio donante trietil-dutiokarbamatojn:
| (C2H5)3N + CS2 + KOH → (C2H5)3NC(S)SK + H2O
|
Literaturo
- Chemical Book
- Merck Millipore
- Encyclopedia.com
- Environmental and Occupational Medicine, William N. Rom, Steven B. Markowitz
- Comprehensive Organic Functional Group Transformations, Volume 6, Alan R. Katritzky, Thomas L. Gilchrist, Otto Meth-Cohn, Charles Wayne Rees
- A Comprehensive Guide to the Hazardous Properties of Chemical Substances, Pradyot Patnaik


