| Dukalia hidrogena fosfato | |||
 | |||
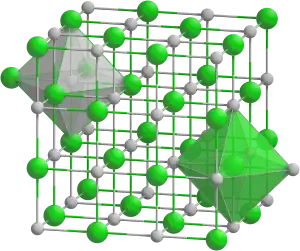
| Plata kemia strukturo de la Kalia fosfato dubaza | |||
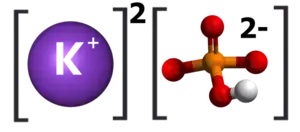 | |||
| 3D kemia strukturo de la Kalia fosfato dubaza | |||
 | |||
| Blankaj kristaloj de Kalia fosfato dubaza | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 7758-11-4 | ||
| ChemSpider kodo | 22858 | ||
| PubChem-kodo | 24450 | ||
| Fizikaj proprecoj | |||
| Aspekto | blanka senodora pulvoro | ||
| Molmaso | 174.174 g·mol−1 | ||
| Denseco | 2.44g cm−3 | ||
| Fandpunkto | 340 °C[1] | ||
| Ekflama temperaturo | Nebrulema | ||
| Acideco (pKa) | 2.12 | ||
| Solvebleco | Akvo:1492.5 g/L | ||
| Mortiga dozo (LD50) | 4640 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Riskoj | R35 R36/37/38 | ||
| Sekureco | S26 S36/37/39 S45 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H315, H318 | ||
| GHS Deklaroj pri antaŭgardoj | P264, P280, P302+352, P305+351+338, P310, P321, P332+313, P362[2] | ||
(25 °C kaj 100 kPa) | |||
Kalia fosfato dubaza estas tre solvebla neorganika kombinaĵo de kalio, fosforo, oksigeno kaj hidrogeno. Ĝi estas fosfata salo de kalio, blanka aŭ senkolora substanco, uzata kiel sterko, nutroaldonaĵo, reakciagento kaj bufragento. Ordinare, ĝi estas komerca fonto de fosforo kaj kalio. Biologie ĝi uzatas en la produktado de algoj kiuj ankaŭ estas uzataj en la kulturo de bakterioj.
Sintezoj
Sintezo 1
- Kalia fosfato dubaza estas preparebla per nekompleta interagado de la fosfata acido kaj kalia hidroksido:
|
|
Sintezo 2
- Aŭ per reakcio de fosfata acido kaj kalia karbonato:
|
|
Sintezo 3
- Sed ni ankaŭ povas prepari ĝin per agado de la kalia duhidrogena fosfato kaj kalia hidroksido:
|
|
Reakcioj
Reakcio 1
- Dukalia fosfato malkomponiĝas sub altaj temperaturoj:
|
|
Reakcio 2
- Kun fosfatacido ĝi iĝas duhidrogena fostato de kalio:
|
|
Reakcio 3
- Kun kalia hidroksido ĝi komplete neutraliziĝas:
|
|
Reakcio 4
- Dukalia fostato reakcias kun arĝenta nitrato donante arĝentan fosfaton kaj duhidrogenan fosfaton de kalio:
|
|
Literaturo
Vidu ankaŭ
Referencoj
| ||||||
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.