| Irigenino | ||
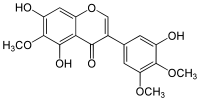 | ||
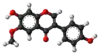
| Plata kemia strukturo de la Irigenino | ||
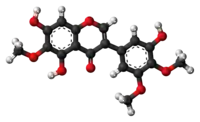 | ||
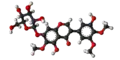
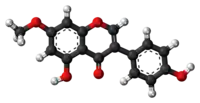
| Tridimensia kemia strukturo de la Irigenino | ||
 | ||
| Irigenino estas flava antioksidigaĵo trovata en plantoj tia kia la Belamcanda chinensis[1] | ||
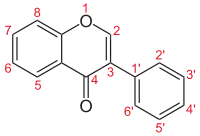 | ||
| Numerigo de la karbonaj strukturoj de la izoflavonoj. | ||
| Kemia formulo | ||
| CAS-numero-kodo | 548-76-5 | |
| ChemSpider kodo | 4576563 | |
| PubChem-kodo | 5464170 | |
| Fizikaj proprecoj | ||
| Aspekto | flava solidaĵo | |
| Molmaso | 360,315 g·mol−1 | |
| Denseco | 1,461g cm−3 | |
| Fandpunkto | 189 °C−192 °C[2] | |
| Bolpunkto | 646,1 °C[3] | |
| Refrakta indico | 1,649 | |
| Ekflama temperaturo | 237,7 °C | |
| Acideco (pKa) | 6,36 | |
| Solvebleco | Akvo:0,066 g/L [4] | |
| Sekurecaj Indikoj | ||
| Riskoj | R36/37/38 | |
| Sekureco | S26 S36 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H315, H319, H335 | |
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P321, P332+313, P337+313, P362, P403+233, P405, P501 | |
(25 °C kaj 100 kPa) | ||
Irigenino, (3',5,7-trihidrokso,4',5',6-trimetokso-izoflavono) aŭ C18H16O8 estas natura fitokemiaĵo, flava solidaĵo nesolvebla en akvo kaj trovata en sennombraj plantoj tiaj kiaj Iris domestica,[5], Iris nepalensis[6] kaj "Iris hookeriana". Irigenino estas antiinflama, antioksidiga, antimalaria kaj antitumora substanco.[7]. La glukozido de la irigenino havas la samajn efikojn, estas amargusta kaj uzata en la traktado de gorĝaj infektaĵoj.
Sintezoj
Sintezo 1
- Preparado ekde la gliciteino per aldono de hidroksila grupo en la 5-a pozicio de la kromenonila grupo, interŝanĝo de la hidroksila grupo je metoksila grupo en la 4-a pozicio de la fenila grupo, aldono de hidroksila grupo en la 3-a pozicio kaj metoksila grupo en la pozicio 5-a de la fenila grupo:
|
|
Sintezo 2
- Preparado per hidratigo de la iridino:
|
|
Sintezo 3
- Preparado ekde la kalikozino per aldono de hidroksila grupo en la 5-a pozicio de la kromenonila grupo, aldono de metoksila grupo en la 6-a pozicio de la kromenonila grupo, kaj aldono de metoksila grupo en la 5-a pozicio de la fenila grupo:
|
|
Sintezo 4
- Preparado ekde la pratenseino per aldono de metoksila grupo en la 6-a pozicio de la kromenonila grupo, kaj aldono de metoksila grupo en la 5-a pozicio de la fenila grupo:
|
|
Sintezo 5
- Preparado ekde la prunetino per aldono de metoksila grupo en la 6-a pozicio de la kromenonila grupo, interŝanĝo de la metoksila grupo je hidroksila grupo en la 7-a pozicio de la kromenonila grupo, aldono de hidroksila grupo en la 3-a pozicio de la fenila grupo, interŝanĝo de la hidroksila grupo je metoksila grupo en la 4-a pozicio de la fenila grupo kaj aldono de metoksila grupo en la 5-a pozicio de la fenila grupo:
|
|
Sintezo 6
- Preparado ekde la retuzino per aldono de hidroksila grupo en la 5-a pozicio de la kromenonila grupo, aldono de metoksila grupo en la 6-a pozicio de la kromenonila grupo, forigo de hidroksila grupo en la 8-a pozicio de la kromenonila grupo, aldono de hidroksila grupo en la 3-a pozicio de la fenila grupo, kaj aldono de metoksila grupo en la 5-a pozicio de la fenila grupo:
|
|
Sintezo 7
- Preparado ekde la tektorigenino per forigo de hidroksila grupo en la 3-a pozicio de la fenila grupo, interŝanĝo de la hidroksila grupo je metoksila grupo en la 4-a pozicio de la fenila grupo kaj aldono de metoksila grupo en la 5-a pozicio de la fenila grupo:
|
|
Reakcioj
Reakcio 1
- Konvertado al gliciteino per forigo de hidroksila grupo en la 5-a pozicio de la kromenonila grupo, interŝanĝo de la metoksila grupo je hidroksila grupo en la 4-a pozicio de la fenila grupo, forigo de hidroksila grupo en la 3-a pozicio kaj metoksila grupo en la pozicio 5-a de la fenila grupo:
|
|
Reakcio 2
- Konvertado al iridino per senhidratigo:
|
|
Reakcio 3
- Konvertado al kalikozino per forigo de hidroksila grupo en la 5-a pozicio de la kromenonila grupo, forigo de metoksila grupo en la 6-a pozicio de la kromenonila grupo, kaj forigo de metoksila grupo en la 5-a pozicio de la fenila grupo:
|
|
Reakcio 4
- Konvertado al pratenseino per forigo de metoksila grupo en la 6-a pozicio de la kromenonila grupo, kaj forigo de metoksila grupo en la 5-a pozicio de la fenila grupo:
|
|
Reakcio 5
- Konvertado al prunetino per forigo de metoksila grupo en la 6-a pozicio de la kromenonila grupo, interŝanĝo de la hidroksila grupo je metoksila grupo en la 7-a pozicio de la kromenonila grupo, forigo de hidroksila grupo en la 3-a pozicio de la fenila grupo, interŝanĝo de la metoksila grupo je hidroksila grupo en la 4-a pozicio de la fenila grupo kaj forigo de metoksila grupo en la 5-a pozicio de la fenila grupo:
|
|
Reakcio 6
- Konvertado al retuzino per forigo de hidroksila grupo en la 5-a pozicio de la kromenonila grupo, forigo de metoksila grupo en la 6-a pozicio de la kromenonila grupo, aldono de hidroksila grupo en la 8-a pozicio de la kromenonila grupo, forigo de hidroksila grupo en la 3-a pozicio de la fenila grupo, kaj forigo de metoksila grupo en la 5-a pozicio de la fenila grupo:
|
|
Reakcio 7
- Konvertado al tektorigenino per forigo de hidroksila grupo en la 3-a pozicio de la fenila grupo, interŝanĝo de la metoksila grupo je hidroksila grupo je en la 4-a pozicio de la fenila grupo kaj forigo de metoksila grupo en la 5-a pozicio de la fenila grupo:
|
|
Literaturo
- Cancer Inhibitors from Chinese Natural Medicines
- Science Direct
- Nature
- Alcohols—Advances in Research and Application
- Cell Biology and Instrumentation: UV Radiation, Nitric Oxide and Cell Death ...
- RÖMPP Encyclopedia Natural Products
- Flavonoids: From Biosynthesis to Human Health
- Methods in Plant Biochemistry
Referencoj
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.


-3D-balls.png.webp)