| Fluorometano | |||
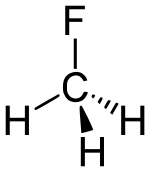 | |||
| Plata kemia strukturo de la Fluorometano | |||
 | |||
| Tridimensia kemia strukturo de la Fluorometano | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 593-53-3 | ||
| ChemSpider kodo | 11148 | ||
| PubChem-kodo | 11638 | ||
| Merck Index | 15,4206 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora gaso | ||
| Molmaso | 34,033 g·mol−1 | ||
| Fandpunkto | −141,8 °C | ||
| Bolpunkto | −78,2 °C | ||
| Refrakta indico | 1,727 | ||
| Solvebleco | Akvo:2,295 g/L | ||
| Sekurecaj Indikoj | |||
| Riskoj | R12 | ||
| Sekureco | S9 S16 S23 S24/25 S26 S28 S33 S36/37/39 S60 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H220, H280 | ||
| GHS Deklaroj pri antaŭgardoj | P210, P377, P381, P403, P401, P403[1] | ||
(25 °C kaj 100 kPa) | |||
Fluorometano aŭ CH3F, ankaŭ konata kiel metila fluorido, estas netoksa, likvigebla kaj bruligebla senkolora gaso sub normaj kondiĉoj je temperaturo kaj premo. Ĝi devenas el la metano kie unu hidrogenatomo estis anstataŭita de unu fluora atomo.
Ĉar fluorometano estas kemie kaj biologie inerta kaj malalte toksa, specifa aktiveco ne estas zorgo en la preparado por homa uzo. Fluorometano estas uzata kiel mekanismo por taksado de la sangofluo en la cerbo.[2]
Sintezoj
Sintezo 1
- Preparado de fluorometano per kataliza interagado de metanolo kaj fluorida acido
|
|
Sintezo 2
- Preparado de fluorometano per kataliza interagado de klorometano kaj dufluorido de duhidrogeno:
|
2 |
Sintezo 3
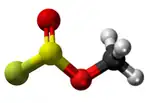
- Preparado de fluorometano per makomponado de metila fluoro-sulfinato:
|
|
Sintezo 4
- Preparado de fluorometano per interagado de jodoformo kun fluorida acido:
|
|
Sintezo 5
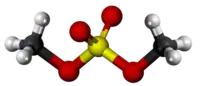
- En 1835, Jean-Baptiste Dumas (1800-1884) preparis fluorometanon per traktado de dumetila sulfato kun kalia fluorido:[3]
|
|
Reakcioj
Reakcio 1
- Fluorometano reakcias kun kalia hidrido por doni metanon:[4]
|
|
Reakcio 2
- Acetonitrilo estas preparebla per interagado de fluoro-metano kun kalia cianido:
|
|
Reakcio 3
- Metanolo estas preparebla per interagado de fluoro-metano kun natria hidroksido:
|
|
Literaturo
Vidu ankaŭ
Referencoj
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.