| Fluorata acido | |
 | |
 | |
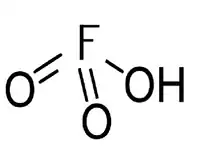
Fluorata acido aŭ HFO3 estas hipoteza oksida acido de fluoro, molekula maso 68 g/molo, gasa substanco kiu povas dissolvi silikon, kaj konservi ĝin pendanta en la gasa stato. Do, ĝi dissolvas glasojn, kristalojn kaj plurajn multekostajn ŝtonojn. Ĝi estas pli peza ol la atmosfera aero, ne estas brulema, kaj estas venena kiam enspirita. La hidrogena fluorato miksita kun akva solvaĵo estigas fluoratan acidon. Ĝia odoro estas penetranta kaj iom simila al tiu de la klorida acido.
Ĝi korodas bestajn kaj vegetalajn materialojn kaj la lumo ne havas efekton sur ĝin. Ĝi eligas blankajn fumojn en la humida atmosfero. Ĝi estas forte acida kaj do ruĝigas organikajn vegetalojn. Ĝi precipitas kalcian hidroksidon kaj ne reakcias kun platino, oro, arĝenta hidrargo, stano, plumbo, antimono, kobalto, nikelo kaj bismuto, sed reakcias kun fero, arseno kaj mangano[1]. Fluorata acido estas preparebla reakciante "natria fluorato" kun sulfata acido kaj ne povas esti konservita en vitraĵoj.
2 NaFO3 + H2SO4 → Na2SO4 + 2 HFO3
Mineralaj acidoj
| Halogenidaj acidoj | |||||||
| HF | Fluorida acido | HCl | Klorida acido | HBr | Bromida acido | HI | Jodida acido |
| HFO | Hipofluorita acido | HClO | Hipoklorita acido | HBrO | Hipobromita acido | HIO | Hipojodita acido |
| HFO2 | Fluorita acido | HClO2 | Klorita acido | HBrO2 | Bromita acido | HIO2 | Jodita acido |
| HFO3 | Fluorata acido | HClO3 | Klorata acido | HBrO3 | Bromata acido | HIO3 | Jodata acido |
| HFO4 | Perfluorata acido | HClO4 | Perklorata acido | HbrO4 | Perbromata acido | HIO4 | Perjodata acido |
Literaturo
- A Dictionary of Chemistry, on the Basis of Mr. Nicholson's: In ..., Volume 1, Andrew Ure
- Encyclopædia Americana, Volume 5, Francis Lieber, Edward Wigglesworth, Thomas Gamaliel Bradford, Henry Vethake
- EndMemo
- Process for dissolving tin and tin alloys
- The Monthly Review, Ralph Griffiths, George Edward Griffiths
- A dictionary of chemistry and mineralogy: with an account of the ..., Volume 2, Arthur Aikin, Charles Rochemont Aikin
Vidu ankaŭ


Fluoroborata acido 


H3OBF4 