| Kloroetano | |||||
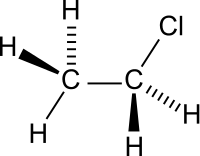 | |||||
| Plata kemia strukturo de la Kloroetano | |||||
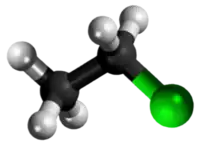 | |||||
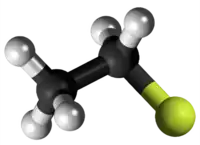
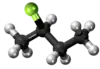
| Tridimensia kemia strukturo de la Kloroetano | |||||
| Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | |||||
| CAS-numero-kodo | 75-00-3 | ||||
| ChemSpider kodo | 6097 | ||||
| PubChem-kodo | 6337 | ||||
| Merck Index | 15,3837 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | senkolora, potence toksa, brulema gaso kun karakteriza tranĉe etera odoro | ||||
| Molmaso | 64,512 g·mol−1 | ||||
| Denseco | 0,921g cm−3 | ||||
| Fandpunkto | −138 °C | ||||
| Bolpunkto | 12,3 °C | ||||
| Refrakta indico | 1,3676[1] | ||||
| Ekflama temperaturo | −43 °C[2] | ||||
| Memsparka temperaturo | 510 °C | ||||
| Solvebleco | Akvo:5,7 g/L | ||||
| Sekurecaj Indikoj | |||||
| Riskoj | R12 R40 R52/53 | ||||
| Sekureco | S9 S16 S33 S36 S37 S61 | ||||
| Pridanĝeraj indikoj | |||||
| Danĝero
| |||||
| GHS Damaĝo Piktogramo |
| ||||
| GHS Signalvorto | Damaĝa substanco | ||||
| GHS Deklaroj pri damaĝoj | H220, H280, H315, H319, H336, H351, H370, H371, H372, H402, H412 | ||||
| GHS Deklaroj pri antaŭgardoj | P201, P202, P210, P260, P261, P264, P270, P271, P273, P280, P281, P302+352, P304+340, P305+351+338, P314, P321, P332+313, P337+313, P362, P377, P381, P403, P403+233, P405, P410+403, P501[3] | ||||
(25 °C kaj 100 kPa) | |||||
Kloroetano aŭ C2H5Cl estas organika komponaĵo, rezultanta el kompleta interagado de etanolo kaj klorida acido, senkolora, potence toksa, alte brulema gaso kun karakteriza tranĉe etera aŭ dolĉeca odoro, uzata en kemiaj sintezoj kaj kiel reakciaĵo en laboratorioj. Ĝi uzatas en la produktado de plumba kvaretilo (iu benzina aldonaĵo), anesteziloj, insekticidoj, fridigado, kaj kiel solvanto por grasaĵoj, oleoj kaj ciroj.
Malgraŭ ke ĝi estas la malpli toksa el la klorhavaj hidrokarbonidoj, ĝi povas kaŭzi nelongedaŭran narkozon. Ĝi povas absorbiĝi per haŭto, okuloj kaj mukoza membrano. Ĝi estas milde toksa per ingestado. Akuta venenigo povas afekti hepaton, renojn, spirsistemon kaj koron.
Sintezoj
Sintezo 1
|
|
Sintezo 2
- Preparado per interagado de etileno kaj klorida acido:
|
|
Sintezo 3
- Preparado per trakatado de etanolo kaj klorida acido:
|
|
Sintezo 4
- Preparado per reakcio inter fluoroetano kaj kalcia klorido:
|
2 |
Sintezo 5
- Preparado per reakcio inter tionila klorido kaj etanolo:
|
|
Sintezo 6
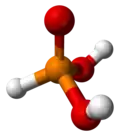
- Preparado per reakcio inter etanolo kaj fosfora triklorido:
|
3 |
Sintezo 7
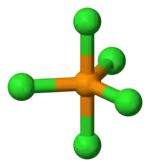
- Preparado per reakcio inter etanolo kaj fosfora kvinklorido:
|
|
Reakcioj
Reakcio 1
- Preparado de kvaretila plumbo:
|
4 |
Reakcio 2
- Reakcio kun natria hidroksido:
|
|
Reakcio 3
- Reakcio kun acetileno
|
|
Reakcio 4
- Reakcio kun etileno
|
|
Reakcio 5
- Reakcio kun magnezio:
|
|
Reakcio 6
- Reakcio kun zinko en ĉeesto de klorida acido:
|
|
Reakcio 7
- Reakcio kun arĝenta nitrito:
|
|
Reakcio 8
- Reakcio kun amoniako
|
|
Reakcio 9
- Reakcio kun natria jodido:
|
|
Reakcio 10
- Reakcio kun natria hidrogena sulfido:
|
|
Literaturo
Vidu ankaŭ
Referencoj
- ↑ Chemical Book
- ↑ Merck Millipore. Arkivita el la originalo je 2019-01-15. Alirita 2019-01-15.
- ↑ PubChem
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.