| Etila citrato | ||
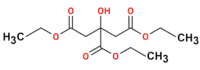 | ||
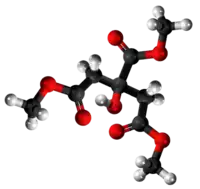
Etila citrato | ||
 | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 77-93-0 | |
| ChemSpider kodo | 13850879 | |
| PubChem-kodo | 6506 | |
| Fizikaj proprecoj | ||
| Aspekto | senkolora brulema likvaĵo[1] | |
| Molmaso | 276,285g mol−1 | |
| Denseco | 1,136 g/cm−3[2][3] | |
| Fandpunkto | -55°C [4] | |
| Bolpunkto | 294°C [5][6] | |
| Refrakta indico | 1,442[7] | |
| Ekflama temperaturo | 95,4°C [8][9] | |
| Solvebleco | Akvo:65 g/L[10] | |
| GHS etikedigo de kemiaĵoj | ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H319 | |
| GHS Deklaroj pri antaŭgardoj | P264, P280, P305+351+338, P337+313 | |
(25 °C kaj 100 kPa) | ||
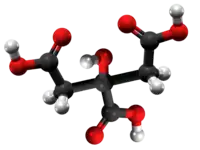
Etila citrato aŭ C12H20O7 estas organika nesaturita kombinaĵo rezultanta el interagado de la citrata acido kun etanolo. Ĝi estas senodora amargusta[11] senkolora likvaĵo uzata en kemiaj sintezoj kaj en polimerizaj reakcioj. Trietila citrato estas solvebla en akvo, acetono, etero, etanolo kaj metanolo. Per hidrolizo ĝi donas etilan alkoholon kaj citratan acidon.
Reakcioj
Reakcio 1
- Preparado de etila citrato per neŭtraligo de la citrata acido kun etila alkoholo:
|
3 |
Reakcio 2
- Preparado de etila citrato per acida transesterigo:
|
3 |
Reakcio 3
- Preparado de etila citrato per estera transesterigo:
|
3 |
Reakcio 4
- Preparado de etila citrato per acida transesterigo:
|
3 |
Reakcio 5
- Hidrolizo de etila citrato:
|
|
Reakcio 6
- Sapigo de etila citrato:
|
|
Vidu ankaŭ
Referencoj
- ↑ Handbook of the Thermodynamics of Organic Compounds
- ↑ Chemnet
- ↑ Chemsrc
- ↑ Chemical Book
- ↑ Chembk
- ↑ Chemblink
- ↑ Sigma Aldrich
- ↑ Chemnet
- ↑ Chemsrc
- ↑ Chuangyingchem.com. Arkivita el la originalo je 2022-03-01. Alirita 2022-03-01.
- ↑ Compendium of Food Additive Specifications
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.