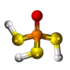| Etanotiolo | ||||
 | ||||
| Plata kemia strukturo de la Etanotiolo | ||||
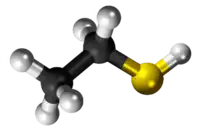 | ||||
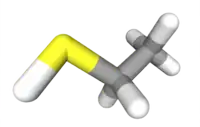
| Tridimensia kemia strukturo de la Etanotiolo | ||||
| Alternativa(j) nomo(j) | ||||
| ||||
| Kemia formulo | ||||
| CAS-numero-kodo | 75-08-1 | |||
| ChemSpider kodo | 6103 | |||
| PubChem-kodo | 6343 | |||
| Fizikaj proprecoj | ||||
| Aspekto | senkolora likvaĵo kun odoro je putra ovo | |||
| Molmaso | 62,13404 g·mol−1 | |||
| Denseco | 0,862g cm−3 | |||
| Fandpunkto | -148 °C[1] | |||
| Bolpunkto | 35 °C | |||
| Refrakta indico | 1,4306[2] | |||
| Ekflama temperaturo | -45 °C | |||
| Acideco (pKa) | 10,6 | |||
| Solvebleco | Akvo:6,8 g/L | |||
| Mortiga dozo (LD50) | 682 mg/kg (buŝe) | |||
| Sekurecaj Indikoj | ||||
| Riskoj | R11 R20 R50/53 | |||
| Sekureco | S16 S25 S60 S61 | |||
| Pridanĝeraj indikoj | ||||
| Danĝero
| ||||
| GHS Damaĝo Piktogramo |
| |||
| GHS Signalvorto | Damaĝa substanco | |||
| GHS Deklaroj pri damaĝoj | H225, H332, H400, H410 | |||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P261, P271, P273, P280, P303+361+353, P304+312, P304+340, P370+378, P391, P403+235, P501[3] | |||
(25 °C kaj 100 kPa) | ||||
Etanotiolo aŭ H3CSH, ankaŭ konata kiel etilmerkaptano estas organosulfura komponaĵo, konsistanta je unu grupo tiolo (-SH) ligita al unu grupo etilo (CH3CH2-), senkolora, toksa gaso kun odoro je putra ovo, trovata en la sango kaj cerbo de homoj kaj bestoj, samkiel en plantaj histoj. Ĝi same nature okazas en bestaj fekaĵoj kaj en kelkaj nutraĵoj tiaj kiaj fromaĝoj kaj nuksoj. Ĝi estas la unu el la ĉefaj komponaĵoj respondecaj pri la malbona buŝ- kaj furz- odoroj. Etanotiolo estas brulema substanco klasita kiel tioalkoholo kaj kelkfoje ĝi estas mallongigita kiel ESH.
Sintezoj
Sintezo 1
- Preparado per reakcio de la acetaldehido kun sulfida acido:
|
|
Sintezo 2
- Preparado per kondensiga reakcio inter etileno kaj sulfida acido:
|
|
Sintezo 3
- Preparado per agado de la etila klorido sur kalia sulfido:
|
|
Sintezo 4
- Preparado per traktado de duetila sulfido kaj sulfida acido:
|
|
Sintezo 5
- Preparado per traktado de la etilamino kaj kalia bisulfido:
|
|
Sintezo 6
- Preparado per reduktigo de la duetila dusulfido:
|
|
Sintezo 7
- Preparado per interagado de la kalia etilsulfato kaj kalia hidrogenosulfido:[4]
|
|
Reakcioj
Reakcio 1
- Reakcio kun POCl3:
|
3 |
Reakcio 2
- Oksidigo de tioetanolo:
|
|
Reakcio 3
- Acida esterigo de tioalkoholoj:
|
|
Reakcio 4
- Anhidrida esterigo de tioalkoholoj:
|
|
Reakcio 5
- Reakcio kun acetila klorido:
|
|
Reakcio 6
- Intramolekula forigo de hidrogena sulfido el la tioetanolo:
|
|
Reakcio 7
- Reakcio de tioetanolo kun jodo:
|
2 |
Literaturo
Referencoj
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.