| Dietila sulfato | |||||
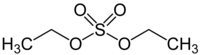 | |||||
| Plata kemia strukturo de la Dietila sulfato | |||||
 | |||||
| Tridimensia kemia strukturo de la Dietila sulfato | |||||
| Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | |||||
| CAS-numero-kodo | 64-67-5 | ||||
| ChemSpider kodo | 5931 | ||||
| PubChem-kodo | 6163 | ||||
| Merck Index | 15,3904 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | koroda, senkolora, oleeca likvaĵo kun malforte pipromento-simila odoro kiu malheliĝas kun la tempopaso | ||||
| Molmaso | 154,18 g·mol-1 | ||||
| Denseco | 1,17g cm−3 | ||||
| Fandpunkto | -25°C | ||||
| Bolpunkto | 209°C | ||||
| Refrakta indico | 1,3989 | ||||
| Ekflama temperaturo | 104 °C[1] | ||||
| Memsparka temperaturo | 436 °C[2] | ||||
| Solvebleco | Akvo:7 g/L (malkomponiĝas) | ||||
| Mortiga dozo (LD50) | 647 mg/kg (buŝe) | ||||
| Sekurecaj Indikoj | |||||
| Riskoj | R45 R46 R20/21/22 R34 | ||||
| Sekureco | S45 S53 | ||||
| Pridanĝeraj indikoj | |||||
| Danĝero
| |||||
| GHS Damaĝo Piktogramo |
| ||||
| GHS Signalvorto | Damaĝa substanco | ||||
| GHS Deklaroj pri damaĝoj | H302, H311, H312, H314, H318, H332, H340, H350 | ||||
| GHS Deklaroj pri antaŭgardoj | P201, P202, P260, P261, P264, P270, P271, P280, P281, P301+312, P301+330+331, P302+352, P303+361+353, P304+312, P304+340, P305+351+338, P308+313, P310, P321, P330, P361, P363, P405, P501[3] | ||||
(25 °C kaj 100 kPa) | |||||
Duetila sulfato aŭ dietila sulfato (ĥemia formulo: (C2H5)2SO4) estas organika kombinaĵo apartenanta al la funkcia grupo de la estero, koroda, senkolora, oleeca likvaĵo kun malforte pipromento-simila[4] odoro kiu malheliĝas kun la tempopaso, uzata en kemiaj sintezoj kaj produktado de sennombraj etilderivaĵoj kaj fabrikado de farboj kaj tekstilaĵoj.
Sulfato de dimetilo estas ankaŭ uzata en la preparado de etilderivaĵoj por fenoloj, aminoj kaj tioloj. Ĝi estas toksa kaj karcinomogena substanco kun iritaj proprecoj al okuloj, haŭto kaj ĝiaj vaporoj estas evitendaj. Ĝi estas sensiva al humideco kaj povas reakcii kun oksidigagentoj. Ĝi estas miksebla kun etanolo, dietila etero kaj kloroformo.
Sintezoj
Sintezo 1
- Preparado per traktado de etileno sur sulfata acido:
|
|
Sintezo 2
- Preparado per traktado de etanolo sur sulfata acido:
|
|
Sintezo 3
- Preparado per interagado de natria sulfato kaj etanolo en ĉeesto de sulfata acido [5]
|
|
Sintezo 4
- Preparado per interagado de klorosulfonata acido kaj etanolo:
|
2 |
Sintezo 5
- Preparado per reakcio inter kalcia sulfato kaj etanolo:
|
2 |
Sintezo 6
- Per termolizo de etila disulfato:
|
2 |
Sintezo 7
- Preparado per traktado de trietila fosfato kaj sulfata acido:
|
2 |
Sintezo 8
- Preparado per traktado de trietila orto-acetato kaj sulfata acido:
|
2 |
Sintezo 9
- Preparado per traktado de trietila arsino kaj sulfata acido:
|
2+3 |
Sintezo 10
- Preparado per reakcio inter etila nitrito kaj klorosulfonata acido
|
2 |
Reakcioj
Reakcio 1
- Reakcio kun kloroetano:
|
|
Reakcio 2
- Reakcio kun natria hidroksido:[6]
|
|
Reakcio 3
- Hidrolizo de dietila sulfato:
|
|
Reakcio 4
- Preparado de duetila karbonato:
|
|
Reakcio 5
- Preparado de 4-etil-fenolo:
|
|
Reakcio 6
- Preparado de trietilamino:
|
|
Reakcio 7
- Reakcio inter duetila sulfato kaj natria hidroksido:
|
2 |
Reakcio 8
- Preparado de metila etanosulfonato:
|
|
Reakcio 9
- Preparado de bromoetano:
|
|
Reakcio 10
- Reakcio kun nitrogena dioksido:
|
|