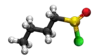| Dubutila dusulfido | ||
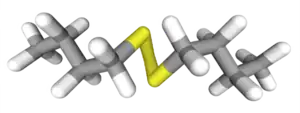 | ||
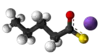
| Bastona kemia strukturo de la Dubutila dusulfido | ||
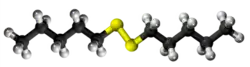 | ||
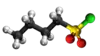
| Tridimensia kemia strukturo de la Dubutila dusulfido | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 629-45-8 | |
| ChemSpider kodo | 10536 | |
| PubChem-kodo | 12386 | |
| Fizikaj proprecoj | ||
| Aspekto | senkolora aŭ blanka likvaĵo kun penetranta malagrabla odoro | |
| Molmaso | 178,3585 g·mol−1 | |
| Denseco | 0,946g cm−3[1] | |
| Fandpunkto | −94 °C[2] | |
| Bolpunkto | 229 °C[3] | |
| Refrakta indico | 1,406 | |
| Ekflama temperaturo | 93 °C[4] | |
| Solvebleco | Akvo:<0,1 g/L | |
| Sekurecaj Indikoj | ||
| Riskoj | R36/37/38 | |
| Sekureco | S26 S37/39 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H315, H319, H335 | |
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P321, P332+313, P337+313, P362, P403+233, P405, P501[5] | |
(25 °C kaj 100 kPa) | ||
Dubutila dusulfido aŭ C8H18S2 estas kemia kombinaĵo, apartenanta al la funkcia grupo de la dusulfidoj de la sulfida acido kaj tiobutanolo. Dubutila dusulfido estas senkolora aŭ blanka likvaĵo kun penetranta malagrabla odoro, analiza reakciaĵo uzata en kemiaj sintezoj kaj en la fabrikado de kosmetikaĵoj kaj farmaciaĵoj. Dubutila dusulfido estas malmulte solvebla en akvo, sed tute solvebla en alkoholo, duetila etero, kloroformo kaj plejmulto el la organikaj solvantoj. Dubutila dusulfido reakcias kun fortaj oksidigagentoj kaj fortaj bazoj. Sulfidaj esteroj malkomponiĝas per varmigo aŭ kun la tempopaso en sulfuro aŭ sulfuraj derivaĵoj.
Sintezoj
Sintezo 1
- Preparado per agado de tiobutanolo kaj jodo:
|
2 |
Sintezo 2
- Preparado per traktado de tiobutanolo kaj bromo:
|
2 |
Sintezo 3
- Preparado per interagado de tiobutanolo kaj sulfura dubromido'':[6]
|
2 |
Sintezo 4
- Preparado per interagado de tiobutanolo kaj sulfura duklorido'':
|
2 |
Sintezo 5
- Preparado per interagado de butano kaj dusulfura dujodido:
|
2 |
Sintezo 6
- Preparado per acida transesterigo inter butano kaj dusulfura dubromido:
|
2 |
Reakcioj
Reakcio 1
- Reduktigo de la dubutila dusulfido:
|
|
Reakcio 2
- Kataliza reakcio kun elementa natrio kaj karbona unuoksido:
|
|
Reakcio 3
- Reakcio kun hidrogena peroksido:
|
|
Reakcio 4
- Reakcio kun klora unuoksido:
|
|
Reakcio 5
- Reakcio kun klora duoksido:
|
|
Literaturo
- The Good Scents Company
- Stenutz
- Evaluation of Certain Food Additives and Contaminants
- Residue Reviews: Residues of Pesticides and Other Contaminants in ...
- Ultraviolet and Visible Absorption Spectra
- Quality of Fresh and Processed Foods
- CRC Handbook of Chemistry and Physics
- Journal of Organic Chemistry of the USSR.
Referencoj
| ||||||
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.