| Anizolo | |||
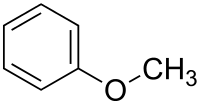 | |||
| Plata kemia strukturo de la Anizolo | |||
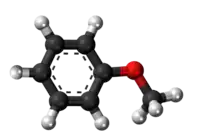 | |||
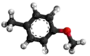
| Tridimensia kemia strukturo de la Anizolo | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 100-66-3 | ||
| ChemSpider kodo | 7238 | ||
| PubChem-kodo | 7519 | ||
| Merck Index | 15,662 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora likvaĵo kun agrabla aromata odoro | ||
| Molmaso | 108,14 g·mol-1 | ||
| Denseco | 0,995g cm−3[1] | ||
| Fandpunkto | −37 °C[2] | ||
| Bolpunkto | 154 °C | ||
| Refrakta indico | 1,5167 | ||
| Ekflama temperaturo | 45,5 °C | ||
| Memsparka temperaturo | 475 °C | ||
| Solvebleco | Akvo:1,71 g/L | ||
| Mortiga dozo (LD50) | 3758 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Riskoj | R10 | ||
| Sekureco | S16 S24 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H226, H315, H319 | ||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P264, P280, P302+352, P303+361+353, P305+351+338, P321, P332+313, P337+313, P362, P370+378, P403+235, P501[3] | ||
(25 °C kaj 100 kPa) | |||
Anizolo, metoksobenzeno, aŭ C7H8O estas organika kombinaĵo apartenanta al la familio de la eteroj, senkolora likvaĵo kun agrabla aromata odoro, uzata en la produktado de sennombraj derivaĵoj, kaj nature trovata en plantoj kaj herboj. Nuntempe ĝi estas sinteze produktata kaj samtempe ĝi estas antaŭajo por sennombraj sintezaj komponaĵoj. Ordinare ĝi estas preparata per la etera sintezo de Williamson kaj ĝi produkteblas laŭ tri eblaj izomeroj (o- m- kaj p-anizolo).
Anizolo estas relative netoksa kaj uzata kiel antaŭaĵo en la fabrikado de parfumoj, insektaj feromonoj kaj farmaciaĵoj. La etera ligilo estas alte stabila sed la metilan grupon oni povas forigi per jodida acido.
Sintezoj
Sintezo 1
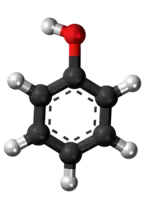
- Preparado per interagado de fenolo kaj dumetila sulfato:
|
2 |
Sintezo 2
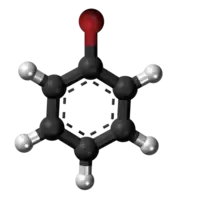
- Preparado per interagado de bromobenzeno kaj natria metoksido
|
|
Sintezo 3
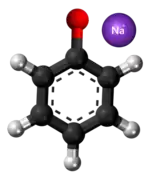
- Metodo de Williamson: Preparado per reakcio inter natria fenoksido kaj klorometano:
|
|
Sintezo 4
- Preparado per reakcio inter fenolo kaj jodometano:
|
|
Reakcioj
Reakcio 1
- Preparado de anetolo per agado de anizolo kun propino:
|
|
Reakcio 2
- Preparado de anizila acetato en tri etapoj: Unue anizolo reakcias kun klorometano por doni metil-anizolon (CAS-numero 104-93-8). Poste, metil-anizolo reakcias kun kloro por formi metokso-benzilan kloridon (CAS-numero 824-94-2) kaj finfine metokso-benzila klorido reakcias kun natria acetato por formi anizilan acetaton.
|
|
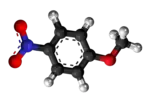
Reakcio 3
- Preparado de p-nitroanizolo (CAS-numero 100-17-4):
|
|
Reakcio 4
- Preparado de anizila acetato en tri etapoj: Unue anizolo reakcias kun bromometano por doni metil-anizolon (CAS-numero 104-93-8). Poste, metil-anizolo reakcias kun bromo por formi metokso-benzilan kloridon (CAS-numero 824-94-2) kaj finfine metokso-benzila klorido reakcias kun natria acetato por formi anizilan acetaton.
|
|
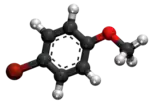
Reakcio 5
- Preparado de bromoanizolo en ĉeesto de acetata acido: [4]
|
|
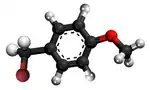
Reakcio 6
- Preparado de anizila alkoholo per interagado de la bromoanizolo kaj natria etoksido:
|
|
Reakcio 7
- Preparado de acetanizolo per interagado de la anizolo kaj acetata anhidrido:
|
|
Reakcio 8
- Preparado de fenolo per forigo de la metila grupo el la anizolo:
|
|
Literaturo
- Hand-book of Chemistry: Organic chemistry Hand-book of Chemistry: Organic chemistry
- Lithium Chemistry: A Theoretical and Experimental Overview
- Heterogeneous Catalysis and Fine Chemicals
- Structure Elucidation in Organic Chemistry: The Search for the Right Tools
- Additive Migration from Plastics Into Food
- Synthetic Methods of Organometallic and Inorganic Chemistry
Vidu ankaŭ
Referencoj
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.