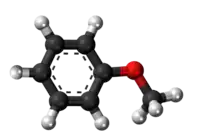
| Anizila bromido | |||
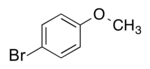 | |||
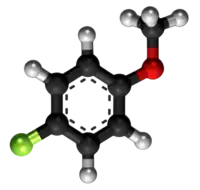
| Plata kemia strukturo de la Anizila bromido | |||
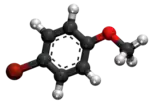 | |||
| Tridimensia kemia strukturo de la Anizila bromido | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 2746-25-0 | ||
| ChemSpider kodo | 144676 | ||
| PubChem-kodo | 165021 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora aŭ flaveca likvaĵo | ||
| Molmaso | 201,063 g·mol-1 | ||
| Denseco | 1,379g cm−3[1] | ||
| Fandpunkto | 10 °C[2] | ||
| Bolpunkto | 241,6 °C[3] | ||
| Refrakta indico | 1,563 | ||
| Ekflama temperaturo | 95,6 °C | ||
| Mortiga dozo (LD50) | 2200 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Riskoj | R34 | ||
| Sekureco | S26 S36/37/39 S45 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H314 | ||
| GHS Deklaroj pri antaŭgardoj | P260, P264, P280, P301+330+331, P303+361+353, P304+340, P305+351+338, P310, P321, P363, P405, P501[4] | ||
(25 °C kaj 100 kPa) | |||
Anizila bromido aŭ C8H9BrO estas organika aromata kombinaĵo, apartenanta al la familia grupo de la bromidoj, senkolora likvaĵo kun penetranta odoro, uzata kiel kemia reakciaĵo en organikaj sintezoj. Ĝi estas produktebla per interagado de la anizila karbinolo kaj bromida acido krom aliaj manieroj. Kiel ĉiuj bromidoj ĝi estas solvebla en akvo kaj iom post iom reakcias kun ĝi. Ĝi prezentas la benzilan ringon inter metoksa grupo (H3C-O-) kaj bromatomo.
Sintezoj
Sintezo 1
- Sintezo per traktado de bromo sur anizila karbinolo:
|
|
Sintezo 2
- Sintezo per traktado de bromida acido sur anizila karbinolo:
|
|
Sintezo 3
- Sintezo per interagado de bromida acido sur anizila klorido:
|
|
Sintezo 4
- Sintezo per interagado de natria bromido sur anizila klorido:
|
|
Sintezo 5
- Sintezo per sapigo de la anizila formiato sekvata per bromigo de la rezultanta anizila karbinolo:
|
|
Sintezo 6
- Sintezo per bromoaminigo de la anizila karbinolo:
|
|
Reakcioj
Reakcio 1
- Hidrolizo de anizila bromido:
|
|
Reakcio 2
- Sapigo de anizila bromido:
|
|
Reakcio 3
- Preparado de anizila klorido:
|
|
Reakcio 4
- Reakcio kun sulfata acido:
|
|
Reakcio 5
- Preparado de anizila acetato:
|
|
Reakcio 6
- Preparado de anizila formiato:
|
|
Reakcio 7
- Reakcio kun hidroksilamino:
|
|
Reakcio 8
- Reakcio kun dumetilzinko:
|
2 |
Reakcio 9
- Preparado de anizilamino:
|
|
Literaturo
Referencoj
| ||||||
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.