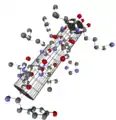
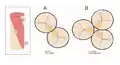
La ĉefa trajto de la alfa-helico estas la volviĝo de la polipeptida ĉeno en spiralan aranĝiĝon, tiel ke hidrogen-ligoj de la speco
\ /
N-H:O=C
/ \
povas formiĝi inter grupoj N-H kaj C=O, kiuj estas tri aŭ kvar aminoacidajn unuojn disaj (averaĝe 3,6 restaĵojn/volviĝo de spiralo).
Plejparto da proteinoj havas helicajn regionojn de diversaj longoj, intermiksitaj kun regionoj de hazarda volvaĵo.
Alfa-helicoj en proteinoj troviĝas kiam sekvo de reziduoj havas la paro de anguloj fi/psi kiu pli malpli egalas -60º/-50º.
En globecaj proteinoj alfa-helicoj konsistas de 4 aŭ 5 ĝis ĉirkaŭ 40 reziduoj, sed la averaĝa longo estas 10 reziduoj (3 volviĝoj). Malkiel DNA kies bazoj direktas H-ligojn al la kerno/interno de la duobla helico kaj fosfat-grupoj ekstere, alfa-helicoj en proteinoj havas H-ligojn direktitaj al la reziduo en la sama pozicio de alia volviĝo (unuope supren kaj malsupren) kaj la flankajn-grupojn direktitaj al la ekstero de la helico.
Pro tiu direkto de la flank-grupoj al la ekstero de alfa-helicoj, kiam alfa-helico havas sian surfacon direktita al akvaĵaj solvaĵoj, la reziduoj estas averaĝe hidrofilaj kaj kiam la surfaco direktigas al ne-akvaĵaj solvaĵoj (ekz-e membranoj), la aminoacidoj estas averaĝe hidrofobaj.
Ĝenerale, alanino (Ala, A), glutamato (Glu, G), leŭcino (Leu, L), kaj metionino (Met, M) estas bonaj stabiligaj aminoacidoj por alfa-helicoj, malkiel prolino (Pro, P), glicino (Gly, G), tirozino (Tyr, T), kaj serino (Ser, S), kiuj estas malbonaj.
Eksteraj ligiloj
- http://www.pnas.org/cgi/content/full/100/20/11207 Arkivigite je 2006-02-27 per la retarkivo Wayback Machine
- http://www2.ufp.pt/~pedros/anim/2frame_helixen.htm Arkivigite je 2012-07-16 per la retarkivo Wayback Machine