| alfa-Pineno | |||||
-a-Pinen.svg.png.webp) | |||||
| Kemia strukturo de la α-Pineno | |||||
-alpha-pinene-3D-balls.png.webp) | |||||
| 3D Kemia strukturo de la α-Pineno | |||||
| Alternativa(j) Nomo(j) | |||||
| |||||
| Kemia formulo | C10H16 | ||||
| PubChem-kodo | 440968 | ||||
| ChemSpider kodo | 389795 | ||||
| CAS-numero-kodo | |||||
| Karakterizaĵoj | |||||
| Aspekto | Senkolora klara likvaĵo | ||||
| Refrakta indico | 1,465[1] | ||||
| Molmaso | 136.23 g·mol−1 | ||||
| Smiles | C\1=C(\[C@@H]2C[C @H](C/1)C2(C)C)C | ||||
| Denseco | 0.858 g/cm3 (20 °C) | ||||
| Viskozeco | 1.303 cP je (25 °C) | ||||
| Fandopunkto | −64 °C (-83 ℉; 209 K) | ||||
| Bolpunkto | 155 °C (311 ℉; 428 K) | ||||
| Solvebleco |
| ||||
| Ekflama temperaturo | 33 °C (91 ℉; 306 °K) | ||||
| Memsparka temperaturo | 491 ℉ (255 °C)[2] | ||||
| Mortiga dozo (LD50) |
| ||||
| Sekurecaj Indikoj | |||||
| Riskoj | R10 R20/21/22 R36/37/38 R43 R51 | ||||
| Sekureco | S16 S26 S36 S37 S60 S61 | ||||
| Pridanĝeraj indikoj | |||||
| Danĝero
| |||||
| GHS etikedigo de kemiaĵoj[4] | |||||
| GHS Damaĝo-piktogramo |
| ||||
| GHS Signalvorto | Damaĝo | ||||
| GHS Deklaroj pri damaĝoj | H226, H304, H315, H317, H411 | ||||
| GHS Deklaroj pri antaŭgardoj | P210, P280, P301, P310, P331, P370+378 | ||||
(25 °C kaj 100 kPa) | |||||
α-Pineno estas organika kombinaĵo de la terpena klaso, kaj izomero de la β-pineno. Ĝi estas alkeno, konata pro ties antisepsaj proprecoj, kaj enhavas forte reakcian kvarmembran ringon. Ĝi estas preskribebla en kazoj de forta bronko-sekrecio. Ĝi estas trovata en oleo de multaj specioj da koniferarboj, ĉefe en la pino. Ĝi same trovatas en la esencoleo de la Rosmarinus officinalis.
Ambaŭ enantiomeroj estas konataj en naturo: (-) α-pineno estas pli konata en Eŭropaj pinarboj, dum (+) -α-izomero estas pli trovata en Nordameriko. La racema miksaĵo ĉeestas en kelkaj oleoj samkiel eŭkaliptoleo kaj oranĝosela oleo. Ĝi ĉeestas same en multenombraj plantoj, tiel kiel mento, esencoleo de lavendo, salvio kaj zingibro. Ĝi ankaŭ trovatas en la esenco de terebintino.
Ĉi-molekulo vigle reakcias kun la dujodo ĉar la aldono de ĉi-halogeno kun la duobla ligo karbona-karbona rezultas en rearanĝo de la karbona strukturo permesante al la organika substrato mildigi la ringotension. La reakcio de la alfa-pineno kun la jodo estas varmoeliga[5] kaŭzante la sublimadon de la jodo. Ĉi-reakcio estis malkovrita de la veterinaro James Herriot (1916-1995). Per la pinoleo trovita en naturo, oni preparas, pere de acida reakcio sur la alfa-pineno, la alfa-terpineolon (C10H18O), kiu konsistigas la ĉefan konstituanton de la pinoleo kaj la molekulo respondeca pri la agrabla odoro je junipero.
La ĉefaj oksidaj produktoj de la alfa-pineno estas la pinenoksido[6], verbenila hidroperoksido[7],verbenolo[8] kaj verbenono[9].
Atmosfera rolo
La unuterpenoj[10], inter kiuj alfa-pineno estas unu el la plej gravaj, elliberiĝas en la atmosfero grandkvante de la vegetaĵaro, kaj ĉi-emisioj estas afekciitaj de la temperaturo kaj lumintenseco. En la atmosfero, la alfa-pineno submetiĝas al reakcioj kun la ozono, la radikalo OH aŭ la radikalo NO3, rezultante en substancoj kun malaltaj volatilecoj kiuj parte kondensiĝas sur la ekzistantaj aerosoloj, tiel generante sekundaraj organikaj aerosoloj. Kelkaj produktoj derivitaj de la alfa-pineno estis eksplicite identigitaj samkiel la pinonaldehido[11], norpinonaldehido[12], pinata acido[13], pinonata acido[14] kaj pinalata acido[15].
Izomeroj de la a-pineno
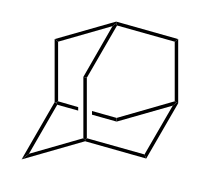
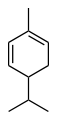
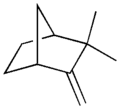
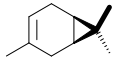
Kareno -Limonen.svg.png.webp)
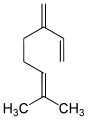
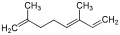
α-Ocimeno 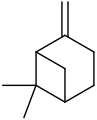
-Sabinene_Structural_Formulea_V.1.svg.png.webp)
Sabineno 
Sintino 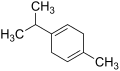
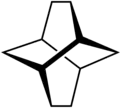
Tuistano 
Referencoj
- ↑ Pinene - Chemie. Arkivita el la originalo je 2015-04-30. Alirita 2015-05-12.
- ↑ PubChem
- ↑ PubChem
- ↑ Sigma Aldrich
- ↑ aŭ ekzoterma
- ↑ Catalysis of Organic Reactions, Frank E. Herkes
- ↑ Preparative Organic Photochemistry, Alexander Schönberg
- ↑ Fortschritte der Chemie organischer Naturstoffe / Progress in the Chemistry ...
- ↑ Does Verbenone Reduce Mountain Pine Beetle Attacks in Susceptible Stands of ...
- ↑ aŭ monoterpenoj
- ↑ Advances in Quantum Chemistry: Applications of Theoretical Methods to ..., John R. Sabin, Erkki J. Brandas
- ↑ Volatile Organic Compounds in the Atmosphere, Ralf Koppmann
- ↑ A System of Chemistry of Inorganic Bodies, Volume 2, Thomas Thomson
- ↑ Handbook on Oleoresin and Pine Chemicals (Rosin, Terpene Derivatives, Tall ..., H. Panda
- ↑ Human Exposure to Pollutants via Dermal Absorption and Inhalation, Mihalis Lazaridis, Ian Colbeck




