Wogonin
Wogonin ist eine chemische Verbindung aus der Gruppe der Flavone.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
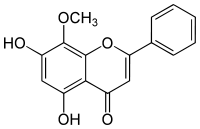 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Wogonin | ||||||||||||
| Andere Namen | |||||||||||||
| Summenformel | C15H10O5 | ||||||||||||
| Kurzbeschreibung |
gelbe Kristalle[2] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 284,26 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Schmelzpunkt |
203–204 °C[3] | ||||||||||||
| Löslichkeit | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Toxikologische Daten | |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Vorkommen

Als natürliches Flavonoid kommt es in der Wurzel des Baikal-Helmkrautes (Scutellaria baicalensis) vor.
Eigenschaften
Wogonin ist ein selektiver COX-2-Hemmer, wodurch es entzündungshemmende Eigenschaften hat. COX-1 wird nicht inhibiert. Die mittlere inhibitorische Konzentration für COX-2 liegt bei 46 µmol. Wogonin zeigt in vivo antioxidative,[6] antivirale,[7] antithrombotische[8] und entzündungshemmende[9] Eigenschaften.[10] Gegenüber Hepatitis-B-Viren ist Wogonin antiviral.[11]
Aufsehen erregte die Entdeckung, dass Wogonin für verschiedene Tumorzellen zytotoxisch ist und die Apoptose (programmierter Zelltod) auslösen kann.[12][13][14] Dagegen ist es bei gesunden Zellen weitgehend ohne Wirkung. Wogonin bewirkt dabei in den entarteten Tumorzellen eine starke Bildung von Wasserstoffperoxid, wodurch die Signalkaskade für die Apoptose initiiert wird.[15][10]
In in-vitro- und in-vivo-Versuchen mit estrogenpositiven und estrogennegativen Mammakarzinomzellen, beziehungsweise Xenografts selbiger auf Nacktmäusen, zeigte Wogonin bei oraler Gabe vielversprechende positive Ergebnisse.[16]
Wogonin wird bislang nicht arzneilich verwendet.
Literatur
- M. Li-Weber: New therapeutic aspects of flavones: the anticancer properties of Scutellaria and its main active constituents Wogonin, Baicalein and Baicalin. In: Cancer Treat Rev 35, 2009, S. 57–68. PMID 19004559.
- J. Peng, Q. Qi, Q. You, R. Hu, W. Liu, F. Feng, G. Wang, Q. Guo: Subchronic toxicity and plasma pharmacokinetic studies on wogonin, a natural flavonoid, in Beagle dogs. In: J Ethnopharmacol 124, 2009, S. 257–262, PMID 19397969.
- H. Z. Piao u. a.: Wogonin inhibits microglial cell migration via suppression of nuclear factor-kappa B activity. In: Int Immunopharmacol 8, 2008, S. 1658–1662, PMID 18725324.
- M. C. Tai u. a.: Therapeutic potential of wogonin: a naturally occurring flavonoid. In: CNS Drug Rev 11, 2005, S. 141–150, PMID 16007236.
Einzelnachweise
- Eintrag zu WOGONIN in der CosIng-Datenbank der EU-Kommission, abgerufen am 23. März 2020.
- Datenblatt Wogonin S. baicalensis (PDF) bei Calbiochem, abgerufen am 9. Dezember 2015.
- P. Singh u. a.: Wogonin, 5,7-dihydroxy-8-methoxyflavone as oestrogenic and anti-implantational agent in the rat. In: Phytotherapy Research 4, 1989, S. 86–89. doi:10.1002/ptr.2650040303.
- Datenblatt Wogonin hydrate bei Sigma-Aldrich, abgerufen am 15. Juni 2011 (PDF).
- Q. Qi u. a.: Toxicological studies of wogonin in experimental animals. In: Phytother Res 23, 2009, S. 417–422. PMID 19003942.
- Z. Gao u. a.: Free radical scavenging and antioxidant activities of flavonoids extracted from the radix of Scutellaria baicalensis Georgi. In: Biochim Biophys Acta 1472, 1999, S. 643–650, PMID 10564778.
- S. C. Ma u. a.: Antiviral Chinese medicinal herbs against respiratory syncytial virus. In: J Ethnopharmacol 79, 2002, S. 205–211, PMID 11801383.
- Y. Kimura u. a.: Effects of flavonoids isolated from scutellariae radix on fibrinolytic system induced by trypsin in human umbilical vein endothelial cells. In: J Nat Prod. 60, 1997, S. 598–601, PMID 9214730.
- Y. S. Chi u. a.: Effects of Wogonin, a plant flavone from Scutellaria radix, on skin inflammation: in vivo regulation of inflammation-associated gene expression. In: Biochem Pharmacol 66, 2003, S. 1271–1278, PMID 14505806.
- S. Baumann u. a.: Wogonin Preferentially Kills Malignant Lymphocytes and Suppresses T-cell Tumor Growth by Inducing PLCgamma1- and Ca2+-dependent Apoptosis. In: Blood 111, 2008, S. 2354–2363. doi:10.1182/blood-2007-06-096198 PMID 18070986.
- C. Wohlfarth und T. Efferth: Natural products as promising drug candidates for the treatment of hepatitis B and C. In: Acta Pharmacol Sin 30, 2009, S. 25–30, PMID 19060918.
- S. Ikemoto u. a.: Antitumor effects of Scutellariae radix and its components baicalein, baicalin, and Wogonin on bladder cancer cell lines. In: Urology 55, 2000, S. 951–955, PMID 10840124.
- Y. C. Chen u. a.: Wogonin and fisetin induction of apoptosis through activation of caspase 3 cascade and alternative expression of p21 protein in hepatocellular carcinoma cells SK-HEP-1. In: Arch. Toxicol. 76, 2002, S. 351–359, PMID 12107653.
- W. R. Lee u. a.: Wogonin and fisetin induce apoptosis in human promyeloleukemic cells, accompanied by a decrease of reactive oxygen species, and activation of caspase 3 and Ca(2+)-dependent endonuclease. In: Biochem Pharmacol 63, 2002, S. 225–236, PMID 11841797.
- Sibylle Kohlstädt: Pflanzeninhaltsstoff mit selektiver Wirkung auf Krebszellen. Deutsches Krebsforschungszentrum, Pressemitteilung vom 17. Dezember 2007 beim Informationsdienst Wissenschaft (idw-online.de), abgerufen am 24. August 2015.
- H. Chung u. a.: Anticancer effects of wogonin in both estrogen receptor-positive and -negative human breast cancer cell lines in vitro and in nude mice xenografts. In: Int J Cancer 122, 2008, S. 816–822, PMID 1795778.