Triphenylphosphanoxid
Triphenylphosphanoxid, veraltet Triphenylphosphinoxid, ist eine organische Phosphorverbindung. Sie besteht aus einem Phosphoratom, an das drei Phenylreste und ein oxidischer Sauerstoff gebunden sind.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
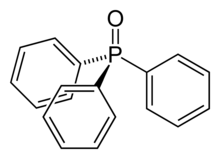 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Triphenylphosphanoxid | |||||||||||||||
| Andere Namen |
Triphenylphosphinoxid | |||||||||||||||
| Summenformel | C18H15OP | |||||||||||||||
| Kurzbeschreibung |
weißer bis gelblicher Feststoff mit unangenehmem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 278,29 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
1,2 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
>360 °C[1] | |||||||||||||||
| Löslichkeit |
schlecht in Wasser[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Herstellung
In der organischen Chemie entsteht Triphenylphosphanoxid in stöchiometrischen Mengen als unvermeidliches „Abfallprodukt“ bei der Wittig-Reaktion, wenn man eine Carbonylverbindung – Aldehyd oder Keton – mit einem Phosphorylid umsetzt, an dessen Phosphoratom drei Phenylgruppen gebunden sind.[1] Es entsteht oft auch als Nebenprodukt in anderen Reaktionen, in denen Triphenylphosphan oder Derivate dessen zum Einsatz kommen, wie beispielsweise in der Appel-Reaktion, der Staudinger-Reaktion oder der Mitsunobu-Reaktion.
Es kann durch Oxidation von Triphenylphosphan mit Sauerstoff hergestellt werden, weshalb auch Triphenylphosphan nach längerem Stehen immer einen Teil Triphenylphosphanoxid enthält.
Eigenschaften
Triphenylphosphanoxid ist ein farbloser Feststoff, der bei 155–158 °C schmilzt. Es ist schlecht löslich in Wasser, Cyclohexan, Tetrachlorkohlenstoff und Acetonitril. Gut löslich ist es hingegen in Dichlormethan, Chloroform und kurzkettigen Alkoholen wie Methanol, Ethanol und 1-Propanol.[2]
Das zentrale Phosphoratom ist tetraedrisch koordiniert. In der energetisch günstigsten Konformation liegen die Phenylreste gegeneinander verdrillt vor.
Triphenylphosphanoxid ist ein guter Ligand für harte Metallzentren.[3]
Die Verbindung zersetzt sich bei höheren Temperaturen. Als Zersetzungstemperatur mit dem Kriterium einer Zersetzungsgeschwindigkeit von 1 mol%·h−1 werden 454 °C angegeben.[4]
Auch beim Erschnüffeln von Datenträgern (Speicherchips etc.) durch Spürhunde spielt Triphenylphosphanoxid eine Rolle.[5]
Einzelnachweise
- Eintrag zu CAS-Nr. 791-28-6 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 25. April 2011. (JavaScript erforderlich)
- E. Maccarone, G. Perrini, Gazz. Chim. Ital. 1982, 112, 447–454.
- D. M. L. Goodgame, M. Goodgame: Near-Infrared Spectra of Some Pseudotetrahedral Complexes of Cobalt (II) and Nickel(II), Inorg. Chem. 1965, 4, 139–143.
- Johns, I.B.; McElhill, E.A.; Smith, J.O.: Thermal Stability of Some Organic Compounds in J. Chem. Eng. Data 7 (1962) 277–281, doi:10.1021/je60013a036.
- Spürhunde erschnüffeln Daten. Abgerufen am 17. November 2019.
