Trimethylboran
Trimethylboran ist eine chemische Verbindung aus der Gruppe der Bororganischen Verbindungen.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
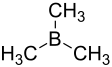 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Trimethylboran | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C3H9B | |||||||||||||||
| Kurzbeschreibung |
farbloses Gas[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 55,92 g·mol−1 | |||||||||||||||
| Aggregatzustand |
gasförmig[1] | |||||||||||||||
| Dichte |
2,318 g·l−1 (21,1˚C)[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
−20,2 °C[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−124,3 kJ/mol[4] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Trimethylboran kann durch Reaktion einer Methyl-Grignard-Reagenz mit Bortrifluorid in einer Di-n-butylether-Lösung unter einer Stickstoffatmosphäre gewonnen werden. Es wird gewöhnlich auch in Form seines Ammoniak-Adduktes NH3:B(CH3)3 dargestellt.[5]
Eigenschaften
Trimethylboran ist ein selbstentzündliches farbloses Gas, das heftig mit Wasser reagiert. Es zersetzt sich bei Erhitzung, wobei an Luft Kohlendioxid, Kohlenmonoxid, Boran und Boroxide entstehen können.[1]
Die Bindungslänge beträgt 157,8 pm (C–B) bzw. 111,4 pm (C–H). Der Bindungswinkel beträgt 120° (CBC) bzw. 112,5° (BCH).[6]
Verwendung
Trimethylboran wird als Vorläufer für Borcarbid-Hartmetall-Dünnfilme durch chemische Gasphasenabscheidung eingesetzt. Es dient auch als Bor-Quelle bei der Abscheidung von Borphosphorsilikatglas (BPSG).[3]
Einzelnachweise
- Eintrag zu Trimethylboran in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- Arkonic: TRIMETHYLBORON
- Datenblatt Trimethylboron, electronic grade, ≥98.35% bei Sigma-Aldrich, abgerufen am 28. Januar 2014 (PDF).
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-25.
- Ross, Gaylon S.; Enagonio, Delmo; Hewitt, Clifford A.; Glasgow, Augustus R.: Preparation of high purity trimethylborane, Journal of Research of the National Bureau of Standards, 1962, Vol. 66A, No. 1, p. 59
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Structure of Free Molecules in the Gas Phase, S. 9-46.


