Trimethylarsinoxid
Trimethylarsinoxid (TMAO) ist eine natürlich vorkommende arsenorganische Verbindung.
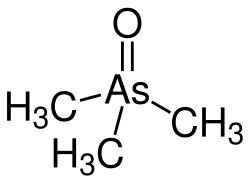
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Trimethylarsinoxid | ||||||||||||
| Summenformel | C3H9AsO | ||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 135,99 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||
| Schmelzpunkt |
188–192 °C[1] | ||||||||||||
| Löslichkeit |
wenig löslich in Wasser[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Toxikologische Daten | |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Vorkommen

Arsenorganische Verbindungen werden von marinen Lebewesen akkumuliert. Bei vielen passiert dies hauptsächlich in Form von Arsenobetain, während Trimethylarsinoxid nur in Spuren auftritt.[2] In einigen Arten macht TMAO jedoch den Großteil des Arsens aus, zum Beispiel in Arten der Ruderfußkrebse, sowie im Büffel-Steuerbarsch und der Welsart Cnidoglanis macrocephalus.[2][3] Zum Teil wird Arsenobetain auch von marinen Mikroorganismen in Sedimenten zu TMAO abgebaut.[4] Es wird angenommen, dass TMAO in biologischen Systemen im Vergleich zu anderen Arsenverbindungen oft in geringen Mengen vorkommt, weil es durch verschiedene Mikroorganismen (u. a. Escherichia coli, Bacillus subtilis und Staphylococcus aureus) schnell zu Trimethylarsin reduziert wird.[5]
Trimethylarsinoxid ist ein metabolisches Zwischenprodukt bei der Umwandlung von Arsenverbindungen wie Arsenat zu Trimethylarsin in Pilzen und Säugetieren (Ratten, Mäusen und Hamstern).[5][6] Terrestrische Organismen enthalten im Allgemeinen deutlich weniger Arsen als marine Organismen, allerdings akkumulieren einige Arten von Pilzen aus der Gattung der Hirschtrüffel (Elaphomyces), z. B. Elaphomyces granulatus, größere Mengen Arsen, wovon bis zu 28 % als TMAO vorliegt.[7] In Pflanzen, die auf einem Arsenvorkommen wachsen, wurden ebenfalls größere Mengen an Arsenverbindungen (darunter TMAO) gemessen. Der Gehalt variierte dabei zwischen verschiedenen Pflanzen, besonders hohe Mengen wurden in Spitzwegerich und Waldsauerklee detektiert.[8] In extremophilen Algen im Yellowstone-Nationalpark wurden Gene untersucht, die für Methyltransferasen kodieren, die methylierte arsenorganische Verbindungen (darunter TMAO) bilden können.[9]
Biosynthese
Die biochemische Umwandlung von Arsenat und Arsenit in Pilzen führt zu über Trimethylarsinoxid zu Trimethylarsin. Arsenat wird zu Arsenit reduziert und dann durch mehrfache Methylierung (vermutlich durch S-Adenosylmethionin) über Methylarsonat und Dimethylarsinat in Trimethylarsinoxid umgewandelt.[6]
Verwendung
Trimethylarsinoxid kommt als Ligand in Komplexen vor, beispielsweise Pentakis(trimethylarsinoxid)-Nickel(II)-Perchlorat, das als Beispielverbindung für Strukturuntersuchungen von High-Spin-Komplexen mit Koordinationszahl fünf verwendet wurde.[10] Es wurden auch Komplexe von TMAO mit Cobalt und Zink beschrieben.[11]
Einzelnachweise
- Eintrag zu Trimethylarsinoxide bei Toronto Research Chemicals, abgerufen am 19. Juni 2023 (PDF).
- D. A. Hunter, W. Goessler, K. A. Francesconi: Uptake of arsenate, trimethylarsine oxide, and arsenobetaine by the shrimp Crangon crangon. In: Marine Biology. Band 131, Nr. 3, 29. Juni 1998, S. 543–552, doi:10.1007/s002270050346.
- J S Edmonds, K A Francesconi: The origin of arsenobetaine in marine animals. In: Applied Organometallic Chemistry. Band 2, Nr. 4, 1988, S. 297–302, doi:10.1002/aoc.590020404.
- Toshikazu Kaise, Ken'ichi Hanaoka, Shoji Tagawa: The formation of trimethylarsine oxide from arsenobetaine by biodegradation with marine microorganisms. In: Chemosphere. Band 16, Nr. 10-12, Januar 1987, S. 2551–2558, doi:10.1016/0045-6535(87)90313-4.
- A Wendy Pickett, Barry C McBride, William R Cullen: Metabolism of trimethylarsine oxide. In: Applied Organometallic Chemistry. Band 2, Nr. 5, 1988, S. 479–482, doi:10.1002/aoc.590020512.
- W.R. Cullen, B.C. McBride, J. Reglinski: The reduction of trimethylarsine oxide to trimethylarsine by thiols: a mechanistic model for the biological reduction of arsenicals. In: Journal of Inorganic Biochemistry. Band 21, Nr. 1, Mai 1984, S. 45–60, doi:10.1016/0162-0134(84)85038-2.
- Simone Braeuer, Jan Borovička, Walter Goessler: A unique arsenic speciation profile in Elaphomyces spp. (“deer truffles”)—trimethylarsine oxide and methylarsonous acid as significant arsenic compounds. In: Analytical and Bioanalytical Chemistry. Band 410, Nr. 9, März 2018, S. 2283–2290, doi:10.1007/s00216-018-0903-3, PMID 29430602, PMC 5849658 (freier Volltext).
- Anita Geiszinger, Walter Goessler, Walter Kosmus: Organoarsenic compounds in plants and soil on top of an ore vein. In: Applied Organometallic Chemistry. Band 16, Nr. 5, Mai 2002, S. 245–249, doi:10.1002/aoc.294.
- Jie Qin, Corinne R. Lehr, Chungang Yuan, X. Chris Le, Timothy R. McDermott, Barry P. Rosen: Biotransformation of arsenic by a Yellowstone thermoacidophilic eukaryotic alga. In: Proceedings of the National Academy of Sciences. Band 106, Nr. 13, 31. März 2009, S. 5213–5217, doi:10.1073/pnas.0900238106, PMID 19276121, PMC 2664070 (freier Volltext).
- Sally H. Hunter, K. Emerson, G. A. Rodley: Structure of pentakis(trimethylarsine oxide)nickel(II) perchlorate. In: Journal of the Chemical Society D: Chemical Communications. Nr. 23, 1969, S. 1398, doi:10.1039/c29690001398.
- A. M. Brodie, S. H. Hunter, G. A. Rodley, C. J. Wilkins: Cobalt(II) complexes with trimethylarsine oxide and trimethylarsine sulphide. In: Journal of the Chemical Society A: Inorganic, Physical, Theoretical. 1968, S. 987, doi:10.1039/j19680000987.


