Tetronsäure
Die Tetronsäure ist eine chemische Verbindung aus der Gruppe der γ-Lactone. Sie entsteht durch Lactonisierung der 4-Hydroxyacetessigsäure.[4] Technisch wird Tetronsäure aus Ethyl-4-chloracetoacetat gewonnen. Sie tritt in mehreren tautomeren Formen auf.
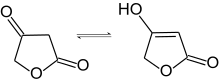 Keto-Enol-Tautomerie der Tetronsäure
Keto-Enol-Tautomerie der Tetronsäure
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
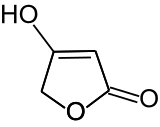 | |||||||||||||||||||
| Strukturformel eines Tautomers (konjugierte Enolform) | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Tetronsäure | ||||||||||||||||||
| Andere Namen |
Furan-2,4-dion | ||||||||||||||||||
| Summenformel | C4H4O3 | ||||||||||||||||||
| Kurzbeschreibung |
farbloser, kristalliner Stoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 100,07 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| pKS-Wert |
3,76[2] | ||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Viele Naturstoffe, wie z. B. Ascorbinsäure oder Penicillansäure besitzen das β-Keto-γ-butyrolacton-Strukturmotiv der Tetronsäure.[2] Tetronsäure kann als Sauerstoff-Analogon der Tetramsäure aufgefasst werden, die ebenfalls Keto-Enol-Tautomerie zeigt.
Einzelnachweise
- Eintrag zu Tetronsäure. In: Römpp Online. Georg Thieme Verlag, abgerufen am 15. August 2013.
- Bertram Barnickel: 3-Funktionalisierung von Tetron- und Tetramsäuren: Beiträge zur Totalsynthese von Bakkenolid-A und Macrocidin A. Bayreuth 2011, DNB 1010489143, S. 13, urn:nbn:de:bvb:703-opus-7699 (Dissertation, Universität Bayreuth).
- Datenblatt Tetronic acid, 96% bei Alfa Aesar, abgerufen am 28. September 2013 (Seite nicht mehr abrufbar).
- Karl-Bernd Walter, Hans-Hartwig Otto: Stickstoffhaltige Derivate der Tetronsäure. In: Arch. Pharm. Band 320, 1987, S. 749–755, doi:10.1002/ardp.19873200814.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.
