Steroid-11β-Hydroxylase
Steroid-11β-Hydroxylase (auch: 11β-Monooxygenase) heißen Enzyme, die die Hydroxylierung von Steroiden an der 11-Position katalysieren. Sie sind unentbehrlich im Steroidhormon-Stoffwechsel von Wirbeltieren und bei der Biotransformation. Im Mensch gibt es zwei 11β-Hydroxylasen: CYP11B1 und CYP11B2. Die Hauptaktivität ist in der Nebenniere (adrenale Steroidsynthese).[1]
| Steroid-11β-Hydroxylase | ||
|---|---|---|
| Masse/Länge Primärstruktur | 503 Aminosäuren | |
| Sekundär- bis Quartärstruktur | mitochondriales Membranprotein | |
| Kofaktor | Häm | |
| Bezeichner | ||
| Gen-Name(n) | CYP11B1, CYP11B2 | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 1.14.15.4, Monooxygenase | |
| Reaktionsart | Hydroxylierung | |
| Substrat | Steroid + red. adr. Ferredoxin + O2 | |
| Produkte | 11beta-Hydroxysteroid + oxid. adr. Ferredoxin + H2O | |
| Vorkommen | ||
| Homologie-Familie | Cytochrom A/B Familie | |
| Übergeordnetes Taxon | Kiefermäuler | |
Im Rahmen einer Enzymkaskade entstehen in der Nebennierenrinde Mineralocorticoide, Glucocorticoide und Sexualhormone. Enzymdefekte in dieser Kaskade führen zu einem Mangel an Cortisol. Dabei werden je nach betroffenem Enzym unterschiedliche alternative Stoffwechselwege beschritten, die zu einer vermehrten Ansammlung unterschiedlicher Steroidhormone führen. Der relativ seltene Mangel an 11β-Hydroxylase führt dabei zu einer seltenen Variante des Adrenogenitalen Syndroms (AGS IV), der CAH durch 11-beta-Hydroxylase-Mangel. Dieses unterscheidet sich von häufigeren Formen des Adrenogenitalen Syndroms durch das Auftreten von zu hohem Blutdruck (Hypertonus) und wird daher auch adrenogenitales Hypertoniesyndrom genannt. Ursächlich dafür ist die gestörte Umwandlung von 11-Desoxykortisol (DOC) zu Aldosteron und der damit verbundene Anstieg von DOC. Dieses wirkt blutdrucksteigernd.
Medikamente wie zum Beispiel Metopiron werden als Hemmer der Steroid-11β-Hydroxylase verwendet.
Katalysierte Reaktion
 + Ferredoxinred. + O2 →
+ Ferredoxinred. + O2 →
→ 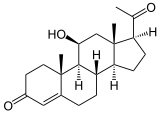 + Ferredoxinox. + H2O
+ Ferredoxinox. + H2O
Progesteron wird zu 11β-Hydroxyprogesteron umgesetzt. Andere natürliche Substrate sind 11-Desoxycortison, 11-Desoxycortisol, Cortison, 18-Hydroxycortison und, im Pilz Absidia coerulea, 16,17α-Epoxyprogesteron.[2]