Phenothiazin
Phenothiazin ist eine chemische Verbindung aus der Gruppe der Thiazine und Namensgeber der Phenothiazine. Sie wurde 1883 von August Bernthsen erstmals synthetisiert.[5]
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
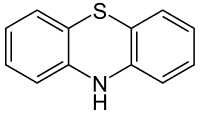 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Phenothiazin | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C12H9NS | ||||||||||||||||||
| Kurzbeschreibung |
gelber Feststoff mit charakteristischem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 199,28 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Dichte |
1,34 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
381 °C (Zersetzung)[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
Schweiz: 5 mg·m−3 (gemessen als einatembarer Staub)[4] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Phenothiazin wird technisch durch katalysierte Umsetzung von Diphenylamin mit 2 Äquivalenten Schwefel als Oxidationsmittel in der Schmelze hergestellt. Dabei entsteht Phenothiazin und als Reduktionsprodukt Schwefelwasserstoff, welches gasförmig abgeführt wird. Das verbleibende Phenothiazin wird durch Vakuumdestillation gereinigt.[5]
Eigenschaften
Phenothiazin ist ein brennbarer, schwer entzündbarer, licht- und luftempfindlicher als Schuppen vorliegender gelber Feststoff mit charakteristischem Geruch, der praktisch unlöslich in Wasser ist. Er zersetzt sich bei Erhitzung.[1] Er oxidiert sehr leicht unter Bildung von 3H-Phenothiazin-3-on, 7-Hydroxy-3H-phenothiazin-3-on und Phenothiazin-5-oxid.[2]
Verwendung
Phenothiazin wird in metallfreien organischen Farbstoffsensibilisatoren, Farbstoffen und Antioxidantien verwendet.[6] Es dient als Antioxidans in Schmiermitteln und Ölen in Konzentrationen bis 1 %, Insektizid, Fungizid, Bakterizid, Ausgangsstoff für die Synthese von Tranquilizern und Antihistaminika, Grundkörper der Thiazinfarbstoffe, als Polymerisationsinhibitor, Medikament (Anthelminthikum) in der Veterinärmedizin, früher auch in der Humanmedizin.[2] Es war das erste synthetische Larvizid, das vor allem in den USA in großem Umfang eingesetzt wurde. Seine Wirksamkeit gegen Moskitolarven wurde 1934 von Campbell und seinen Mitarbeitern entdeckt. Es kann damit als Vorläufer der modernen Insektizide angesehen werden.[7][8]
Sicherheitshinweise
Phenothiazin wirkt beim Menschen und bei Tieren phototoxisch. Die orale und dermale Toxizität von reinem Phenothiazin bei Ratte und Kaninchen ist mit LD50-Werten größer 10.000 mg Phenothiazin/kg Körpergewicht gering. Für die 1-h-LC50 wird ein Wert von mehr als 200.000 mg/m3 angegeben.[2]
Einzelnachweise
- Eintrag zu Phenothiazin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Januar 2023. (JavaScript erforderlich)
- The MAK Collection for Occupational Health and Safety: Phenothiazin (MAK Value Documentation in German language, 2009), doi:10.1002/3527600418.mb9284kskd0046 (freier Volltext).
- Datenblatt Phenothiazine, 98+% bei Alfa Aesar, abgerufen am 18. April 2017 (Seite nicht mehr abrufbar).
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte, abgerufen am 2. November 2015.
- Robert Lee Metcalf: The Mode of Action of Organic Insecticides. National Academies, 1948, S. 44 (eingeschränkte Vorschau in der Google-Buchsuche).
- Datenblatt Phenothiazine, purum, ≥98.0% (GC) bei Sigma-Aldrich, abgerufen am 18. April 2017 (PDF).
- Richard Wegler: Chemie der Pflanzenschutz- und Schädlingsbekämpfungsmittel. Springer Science & Business Media, 2012, ISBN 978-3-642-46210-8, S. 454 (eingeschränkte Vorschau in der Google-Buchsuche).
- Gerhard H. Schmidt: Pestizide und Umweltschutz. Springer-Verlag, 2013, ISBN 978-3-322-83604-5, S. 110 (eingeschränkte Vorschau in der Google-Buchsuche).


