Naphthalinsulfonsäuren
Naphthalinsulfonsäuren sind von Naphthalin abgeleitete chemische Verbindungen mit einer oder mehreren Sulfonsäuregruppen; sie gehören zur Stoffgruppe der aromatischen Sulfonsäuren.[1]
Herstellung
Die Sulfonierung von Naphthalin führt in Abhängigkeit von der Schwefelsäurekonzentration, bzw. der Schwefeltrioxidmenge in der Schwefelsäure (Oleum-Konzentration), sowie den Reaktionsbedingungen zur Bildung von Mono-, Di-, Tri- und Tetrasulfonsäuren. Die Isolierung der einzelnen Sulfonierungsprodukte ist teilweise aufgrund von Desulfonierung und Isomerisierung schwierig. Bei der Sulfonierung von Naphthalin sind neben den beiden Monosulfonsäuren 1-Naphthalinsulfonsäure und 2-Naphthalinsulfonsäure, die sechs Disulfonsäuren 1,3-, 1,5-, 1,6-, 1,7-, 2,6- und 2,7-Naphthalindisulfonsäure, die drei Trisulfonsäuren 1,3,5-, 1,3,6- und 1,3,7-Naphthalintrisulfonsäure, sowie die 1,3,5,7-Naphthalintetrasulfonsäure leicht zugänglich:[1]

Bei der Monosulfonierung handelt es sich um eine reversible elektrophile Substitution.[2] Die 1-Naphthalinsulfonsäure steht über die Ausgangsverbindung im Gleichgewicht mit der 2-Naphthalinsulfonsäure, wobei bei höherer Temperatur das 2-Isomer bevorzugt wird. Bei 160 °C liegt zu 15 % die 1- und zu 85 % die 2-Naphthalinsulfonsäure vor.[3] Nach einer von Henry Edward Armstrong und William Palmer Wynne 1890 aufgestellten Regel nehmen zwei Sulfogruppen am Naphthalingerüst niemals eine ortho-, para- oder peri-Orientierung ein.[4][5]
Eigenschaften
Die Naphthalinsulfonsäuren sind sehr gut wasserlöslich und in Lösung starke Säuren. Die Alkali- und Erdalkalimetallsalze sind ebenfalls wasserlöslich, wobei die Löslichkeit zu den Bariumsalzen hin deutlich abnimmt.[1]
Verwendung
Die Naphthalinsulfonsäuren sind wichtige Zwischenprodukte bei der Herstellung von Farbstoffen, Netz- und Dispergiermittel sowie von Arzneimittel.[2]
Durch Alkalischmelzen erhält man Hydroxynaphthaline und Hydroxynaphthalinsulfonsäuren. Naphthalinsulfonsäuren können zu Nitronaphthalinsulfonsäuren nitriert werden, die sich reduktiv in die entsprechenden Aminonaphthalinsulfonsäuren überführen lassen.[2]

Abhängig von jeweiligen Substitutionsmuster gibt es verschiedene Routen zur Herstellung von Aminohydroxynaphthalinsulfonsäuren. Man erhält diese Verbindungen beispielsweise durch selektive Hydrolyse einer Sulfonsäuregruppe bei Aminonaphthalindi- und Aminonaphthalintrisulfonsäuren wie bei der Synthese von 7-Amino-4-hydroxynaphthalin-2-sulfonsäure (I-Säurae) aus 6-Aminonaphthalin-1,3-disulfonsäure:
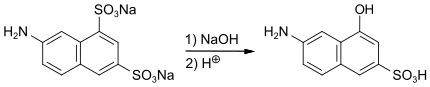
Präparativ schwer zugängliche Aminohydroxynaphthalinsulfonsäuren mit einer ortho-Anordnung der Amino- und Hydroxygruppe erhält man durch Reduktion von Nitroso- oder Arylazoderivaten von Hydroxynaphthalinsulfonsäuren.
Bei der Synthese von Azofarbstoffen werden Hydroxy-, Amino- und Aminohydroxynaphthalinsulfonsäuren als Kupplungskomponente eingesetzt, Amino- und Aminohydroxynaphthalinsulfonsäuren können auch als Diazokomponente verwendet werden.[3]
Einzelnachweise
- Gerald Booth: Naphthalene Derivatives. In: Ullmann’s Encyclopedia of Industrial Chemistry. Band 32. Wiley-VCH Verlag & Co. KGaA, Weinheim, Germany 2000, S. 681 f., doi:10.1002/14356007.a17_009.
- Eintrag zu Naphthalinsulfonsäuren. In: Römpp Online. Georg Thieme Verlag, abgerufen am 30. März 2022.
- Hans Beyer, Wolfgang Walter: Lehrbuch der organischen Chemie. 18. Auflage. S. Hirzel Verlag, Stuttgart 1978, ISBN 3-7776-0342-2, S. 550 ff.
- Proceedings of the Chemical Society, Vol. 6, No. 86. In: Proceedings of the Chemical Society, London. Band 6, Nr. 86, 1890, S. 107–138, doi:10.1039/PL8900600107.
- E. N. Abrahart: Dyes and their Intermediates. 2. Auflage. Edward Arnold Ltd., London 1977, ISBN 0-7131-2580-2, S. 44.
