Meptazinol
Meptazinol (Handelsname Meptid®, Hersteller: Riemser Arzneimittel) ist ein Opioid-Analgetikum für mäßig starke bis starke Schmerzen verschiedener Ursachen. Meptazinol ist neben Tramadol und Nalbuphin eines der drei injizierbaren Opioid-Analgetika, die nicht unter das BtMG fallen. Die analgetische Potenz beträgt das 0,1-fache von Morphin. Es besteht keine Abhängigkeitsentwicklung.[4][5][6]
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||
| 1:1-Gemisch aus (R)-Form (oben) und (S)-Form (unten) | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Meptazinol | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel |
| |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
N02AX05 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | ||||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Klinische Angaben
Anwendungsgebiete (Indikationen)
Meptazinol wird hauptsächlich zur Behandlung des Geburtsschmerzes (zur Kupierung der Wehenschmerzen) eingesetzt. Aufgrund des besseren Nebenwirkungsprofils verdrängt Meptazinol zunehmend Pethidin aus den Kreißsälen.[7] Der entscheidende Vorteil von Meptazinol besteht darin, dass es zu einer selteneren und weniger ausgeprägten Atemdepression der Neugeborenen kommt.[8]
Meptazinol hat seine primären Einsatzbereiche in folgenden Gebieten:[4]
- Behandlung des Wehenschmerzes
- als postoperatives Analgetikum bei schwachen bis mittelstarken Schmerzen
- als Basisanalgetikum im Rahmen einer opioidgestützten Narkose
- wegen der minimalen bis fehlenden Atemdepression als Analgetikum bei akuten, traumatischen Schmerzen im Rahmen der Notfallmedizin
- wegen der fehlenden Vigilanzbeeinträchtigung und einer nur 27%igen Proteinbindung als Analgetikum in der Schmerztherapie des alten Patienten
- wegen der geringen kreislaufstimulierenden, adrenergen Wirkung bei allen Schmerzsituationen mit gleichzeitig starken Blutverlusten
- wegen der antiarrhythmischen Wirkung bei einer gleichzeitig geringen Vigilanzbeeinträchtigung und einer minimalen Proteinbindung als das Analgetikum der Wahl bei mittelstarken Schmerzen alter und sehr alter Patienten
Art und Dauer der Anwendung
Die Dauer der Anwendung richtet sich nach der Schmerzursache, beziehungsweise der Art der Erkrankung. Die Injektion erfolgt intramuskulär oder langsam intravenös.
Gegenanzeigen (Kontraindikationen)
Bei Überempfindlichkeit gegen Meptazinol darf dieses Medikament nicht angewandt werden.
Wechselwirkungen mit anderen Medikamenten
Leberenzyminduzierende Pharmaka können die Wirkung von Meptazinol abschwächen.
Anwendung während Schwangerschaft und Stillzeit
Nicht während der Schwangerschaft anzuwenden, außer zur Linderung von Wehenschmerzen. Beim Neugeborenen ist in seltenen Fällen Atemdepression möglich.
Unerwünschte Wirkungen (Nebenwirkungen)
Zu den möglichen Nebenwirkungen gehören im Wesentlichen Übelkeit und Erbrechen, Müdigkeit bis hin zur Benommenheit und Schwindel, Cephalgien und Magen-Darm-Alterationen.[7]
Pharmakologische Eigenschaften
Wirkungsmechanismus (Pharmakodynamik)
Für die analgetische Wirkung bindet Meptazinol als partieller Agonist den µ1-Opioidrezeptor. Zum µ2-Rezeptor, welcher Atemdepressionen bedingt, existiert dabei nur eine ganz geringe Affinität.[8] Im Unterschied zu anderen Analgetika wird die analgetische Wirkung zusätzlich durch zentral-cholinerge Effekte unterstützt.[9]
Stereoisomerie
Meptazinol enthält ein Stereozentrum, es gibt also zwei Stereoisomere, das (R)-Enantiomer und das spiegelbildliche (S)-Enantiomer. Es ist bekannt, dass Stereoisomere unterschiedliche pharmakologische Wirkungen besitzen.[10] Dennoch wird Meptazinol als Racemat (1:1-Gemisch der beiden Enantiomeren) vermarktet.
Synthese
Eine mehrstufige Synthese von Meptazinol ausgehend von 2-(3-Methoxyphenyl)butyronitril und 4-Iodbuttersäureethylester ist in der Literatur[11] beschrieben. Im zweiten Schritt wird das Nitril zum primären Amin reduziert, das dann zum substituierten Caprolactam cyclisiert. Die Carbonylfunktion des Lactams wird dann mit Lithiumaluminiumhydrid reduziert, es resultiert ein sekundäres heterocyclisches Amin, das am Stickstoff methyliert wird. In der letzten Stufe wird der Methylether gespalten, es entsteht das phenolische Meptazinol als Racemat.
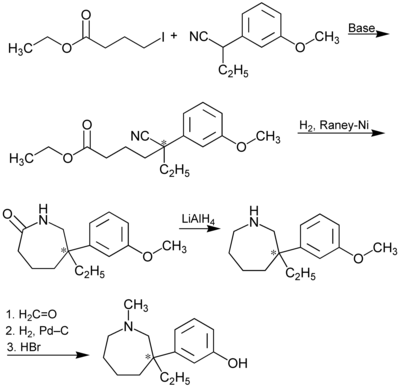
Synthese von racemischem Meptazinol (* = Stereozentrum)
Einzelnachweise
- The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage. 2006, ISBN 0-911910-00-X, S. 1013–1014.
- Eintrag zu Meptazinol. In: Römpp Online. Georg Thieme Verlag, abgerufen am 8. März 2024.
- Datenblatt Meptazinol hydrochloride bei Sigma-Aldrich, abgerufen am 8. März 2024 (PDF).
- Enno Freye: Opioide in der Medizin. 7. Auflage. Springer Medizin Verlag, Heidelberg 2008, S. 314–316.
- P. G. Goode, K. F. Rhodes, J. F. Waterfall: The analgesic and respiratory effects of meptazinol, morphine and pentazocine in the rat. In: J Pharm Pharmacol. 31, 1979, S. 793–795.
- R. E. Johnson, D. R. Jasinski: Human pharmacology and abuse potential of meptazinol. In: Clin Pharmacol Ther. 41, 1987, S. 426–433.
- U. Friebe-Hoffmann, L. Beck: Medikamentöse Analgesie in der Geburtshilfe. In: Gynäkologe. 40, 2007, S. 190–193.
- G. W. Pasternak, A. R. Gintzler, R. A. Houghten, G. S. Ling, R. R. Goodman, K. Spiegel, S. Nishimura, N. Johnson, L. D. Recht: Biochemical and pharmacological evidence for opioid receptor multiplicity in the central nervous system. In: Life Sci. 33 Suppl 1, 1983, S. 167–173.
- D. J. Bill, J. E. Hartley, R. J. Stephens, A. M. Thompson: The antinociceptive activity of meptazinol depends on both opiate and cholinergic mechanisms. In: Br J Pharmacol. 79(1), 1983, S. 191–199.
- E. J. Ariëns: Stereochemistry, a basis for sophisticated nonsense in pharmacokinetics and clinical pharmacology. In: European Journal of Clinical Pharmacology. 26, 1984, S. 663–668, doi:10.1007/BF00541922.
- Axel Kleemann, Jürgen Engel, Bernd Kutscher, Dietmar Reichert: Pharmaceutical Substances. 4. Auflage. 2 Bände. Thieme-Verlag, Stuttgart 2000, ISBN 1-58890-031-2. (seit 2003 online mit halbjährlichen Ergänzungen und Aktualisierungen)