Membrantechnik
Die Membrantechnik umfasst in der Verfahrenstechnik Vorrichtungen und Verfahren zum Transport von Stoffen zwischen zwei Fraktionen unter Zuhilfenahme permeabler Membranen (Trennmembranen).
Es handelt sich um mechanische Trennverfahren zur Separation aus gasförmigen oder flüssigen Stoffströmen.
Anwendungen


Der besondere Vorteil von Membrantrennverfahren ist, dass sie ohne Erhitzen auskommen können und somit meist energetisch günstiger sind als die üblichen thermischen Trennverfahren (Destillation, Sublimation oder Kristallisation). Dieses Trennverfahren ist rein mechanisch und ermöglicht durch seine schonende Trennung die Nutzung beider Fraktionen (Permeat und Retentat). Deshalb hat sich die kalte Separation mittels Membranverfahren insbesondere in der Lebensmitteltechnologie, der Biotechnologie und Pharmazie etabliert. Weiterhin lassen sich mit Hilfe von Membranen Trennungen realisieren, die mit thermischen Verfahren nicht möglich sind, zum Beispiel, weil azeotrope oder isomorphe Kristallisationen eine Trennung durch Destillation oder Umkristallisation unmöglich machen. Je nach Art der verwendeten Membrane ist die selektive Abtrennung einzelner Stoffe oder bestimmter Stoffgemische möglich. Wichtige technische Anwendungen sind die Trinkwassergewinnung durch Umkehrosmose (weltweit etwa 7 Mio. Kubikmeter jährlich), Filtrationen in der Lebensmittelindustrie, die Rückgewinnung von organischen Dämpfen, beispielsweise die Benzindampfrückgewinnung, und die Elektrolyse zur Chlorgewinnung. Aber auch in der Abwasserreinigung wird die Membrantechnologie immer wichtiger. Mit Hilfe der UF und MF (Ultra-/Mikrofiltration) ist es möglich, Partikel, Kolloide und Makromoleküle zu entfernen, so dass Abwasser auf diesem Wege desinfiziert werden kann. Dies ist nötig, falls Abwasser in besonders sensible Vorfluter oder in Badeseen eingeleitet werden soll.
Etwa die Hälfte des Marktes hat Anwendungen in der Medizin. Als künstliche Niere zur Entfernung giftiger Stoffe durch Blutwäsche und als künstliche Lunge durch blasenfreies Zuführen von Sauerstoff in das Blut. Auch bei modernen Energiegewinnungstechniken kommen Membranen immer häufiger zum Einsatz, so zum Beispiel in der Brennstoffzelle und im Osmosekraftwerk.
Stofftransport
Für den Stofftransport an der Membran werden zwei grundlegende Modelle unterschieden: Das Lösungs-Diffusions-Modell und das hydrodynamische Modell. Bei realen Membranen können diese beiden Transportmechanismen durchaus nebeneinander auftreten, insbesondere bei der Ultrafiltration.
Lösungs-Diffusions-Modell
Der Transport erfolgt durch Diffusion, wozu die zu transportierende Komponente zunächst in der Membran gelöst sein muss. Dieses Prinzip überwiegt bei dichten Membranen ohne echte Poren, wie sie bei der Umkehrosmose und der Gastrennung eingesetzt werden. Während des Filtrationsvorgangs bildet sich an der Membran eine Grenzschicht aus. Dieses Konzentrationsgefälle entsteht durch Moleküle, die die Membran nicht passieren können. Dieser Effekt wird als Konzentrationspolarisation[1] bezeichnet; tritt er während der Filtration auf, wird der Transmembranfluss (Flux) reduziert. Die Konzentrationspolarisation ist grundsätzlich umkehrbar – wird die Membran gewaschen, so kann der ursprüngliche Flux nahezu wiederhergestellt werden. Auch das Anlegen eines Querstroms an die Membran (Tangentialflussfiltration) minimiert die Konzentrationspolarisation.
Hydrodynamisches Modell
Transport durch Poren – im einfachsten Fall erfolgt der Transport rein konvektiv. Dafür muss die Größe der Poren kleiner sein als der Durchmesser der abzutrennenden Bestandteile. Membranen, die nach diesem Prinzip funktionieren, werden hauptsächlich bei der Mikro- und Ultrafiltration verwendet; sie werden vor allem eingesetzt, um Makromoleküle aus einer Lösung, Kolloide aus einer Dispersion oder Bakterien abzutrennen. Dabei werden die nicht passierenden Teilchen oder Moleküle auf der Membran in einer mehr oder weniger breiartigen Masse (Filterkuchen) konzentriert (Kuchenfiltration). Wird durch das Zusetzen der Membran die Filtration behindert, kann das sogenannte Querstromverfahren (Tangentialflussfiltration) Abhilfe schaffen. Hierbei strömt die zu filtrierende Flüssigkeit an der Vorderseite der Membran entlang und wird durch die Druckdifferenz zwischen ihrer Vorder- und Rückseite in die Fraktionen Retentat (abströmendes Konzentrat) und Permeat (Filtrat) zerlegt. Dabei entsteht eine Schubspannung, die die Filterkuchenbildung (Deckschichtbildung oder das Fouling) stark einschränkt.
Membrangeometrien und Herstellung

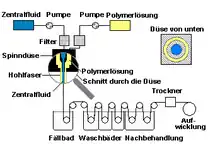
Es werden je nach Anwendung unterschiedliche Filtermembrangeometrien verwendet. Die klassische Form stellt dabei die Flachmembran dar. Dies sind poröse Folien aus Polymer oder keramische Scheiben, die gerakelt oder gegossen werden. Sie werden konstruktionsbedingt meist Dead-End angeströmt. Daneben kommt die kapillarartige Hohlfasermembran sehr oft zum Einsatz, wie sie zum Beispiel im Dialysator verbaut wird. Sie wird meist im Nassspinnverfahren hergestellt. Obwohl es sich bei ihr anbietet, sie im Querstrom-Prinzip – Cross-Flow – anzuströmen, wird sie immer häufiger auch Dead-End angeströmt. Von Bedeutung sind die Wickelmodule, wie sie oft bei der Umkehrosmose oder der Nanofiltration verwendet werden. Dies sind zwei Flachmembranlagen, die durch Gewebe voneinander getrennt sind und spiralförmig aufgewickelt werden. Außerdem gibt es Multikanalelemente – extrudierte, keramische Zylinder (oder Platten) – , die durch innen beschichtete Kanäle durchströmt werden. Bei der sogenannten Composite-Membran wird auf eine poröse Trägerschicht (z. B. MF-Membran) eine aktive Membranschicht aufgetragen. Somit kann die Dicke der aktiven Schicht bei gleich bleibender mechanischer Stabilität verringert werden. Um eine höhere Trennleistung bei Filtern zu erzielen, werden diese mit einer feinporigeren Membranschicht versehen. Bei Polymersystemen verwendet man dafür oft eine Beschichtung mit Silikon, bei keramischen Systemen den Sol-Gel-Prozess. Andere Herstellungsverfahren sind die Grenzflächenkondensation (aromatisches Polyamid auf Träger) oder die Kernspurätzung (Beschuss dünner Filme aus Polycarbonat mit schweren Teilchen eines Beschleunigers).
Polymermembranen
Der überwiegende Teil der kommerziellen Membranen besteht aus Polymeren. Dabei kommt eine Vielzahl verschiedener Kunststoffe zum Einsatz, an die je nach Anwendungsgebiet sehr unterschiedliche Ansprüche gestellt werden. Die beiden verbreitetsten Formen stellen die Wickelmembranen und Hohlfasern dar.
Durch Extrudieren von sehr dünnen Polymerschichten ist es möglich, sehr dünne Schichten (10 Mikrometer) herzustellen. Durch nachfolgendes Aufbringen von chemisch anders gestalteten Polymeren und Wiederholung des Prozesses können verschiedene alternierende Polymerschichten erzeugt werden.
Durch bestimmte Verfahren lassen sich nun sehr kleine Mikrorisse in die Polymerschicht einbringen, wobei die Schicht beispielsweise für Bakterien unpassierbar bleibt.[2] Solche Polymere können für Membranen zur Mikrofiltration verwendet werden.
Lipophile Polymermembranen können den Durchtritt einiger Gase oder organischen Stoffe gestatten, sind jedoch unpassierbar für Wasser und wässrige Lösungen. Derartige Polymere werden beispielsweise in wasserabweisender Regenkleidung, bei medizinischen Geräten oder bei applizierten Arzneimitteln verwendet.[2]
Statt Mikrorissen in Polymerschichten können jedoch auch ionische Gruppen in einem Polymer die Passage von Ionen durch die Membran verhindern. Derartige Membranen werden beispielsweise in der Elektrodialyse eingesetzt.
Andere Membranen sind nur für Wasser und bestimmte Gase durchlässig. Solche Membranen können in der Meerwasserentsalzung oder zur Abtrennung des Sauerstoffs aus der Luft (Gastrennung) eingesetzt werden.[2]
Keramische Membranen
Neben den einfachen Gießlingen aus Schlicker finden hauptsächlich Multikanalelemente Anwendung. Diese extrudierten Elemente finden vor allem in Bereichen Anwendung, die entweder hohe chemische oder thermische Ansprüche an den Filter stellen. Allerdings finden keramische Membranen zunehmend Einzug in die Wasserfiltration, da die hohe Lebenserwartung und die gesunkenen Herstellungskosten ihren Einsatz zunehmend wirtschaftlich gestalten.
 Hohlfasermodul (Dialysator)
Hohlfasermodul (Dialysator) Wickelmodul für die Umkehrosmose
Wickelmodul für die Umkehrosmose Aufgeschnittenes Wickelmodul
Aufgeschnittenes Wickelmodul.jpg.webp) Keramische Multikanalelemente
Keramische Multikanalelemente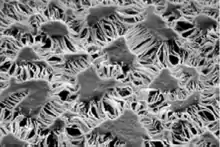
 Durch Kernspurätzung hergestellte Membran
Durch Kernspurätzung hergestellte Membran 0,22 µm Spritzenfilter
0,22 µm Spritzenfilter
Häufig verwendete Membranwerkstoffe
Häufig verwendet werden: Polysulfone, Polyethersulfon (PES) Cellulose, Celluloseester (Celluloseacetat, Cellulosenitrat), Regenerierte Cellulose (RC), Silikone, Polyamide („Nylon“, genauer: PA 6, PA 6.6, PA 6.10, PA 6.12, PA 11, PA 12), Polyamidimid, Polyamid Harnstoff, Polycarbonate, Keramik, Edelstahl, Silber, Silizium, Zeolithe (Alumosilicate), Polyacrylnitril (PAN), Polyethylen (PE), Polypropylen (PP), Polytetrafluorethylen (PTFE), Polyvinylidenfluorid (PVDF), Polyvinylchlorid (PVC), Polypiperazinamid.
Kombinationen aus diesen Werkstoffen werden verwendet, um Dünnschichtmembranen („TF“, englisch „thin film“), häufig aus einer Stützschicht (z. B. Celluloseacetat) und einem Überzug (z. B. Polyamid[3]) herzustellen.
Die Werkstoffwahl hängt von der Trenn- oder Konzentrieraufgabe und dem gewünschten Durchfluss pro Membranfläche und Stunde [l/(m²·h·bar)], sowie der nötigen Ausbeute oder dem maximalen Verlust ab. Auch das zu verwendende Lösungsmittel nimmt Einfluss auf die Trennleistung der Membran. Hydrophile Membranen stoßen tendenziell hydrophobe Stoffe ab und umgekehrt. Allerdings retardieren die hydrophilen Membranen die polaren Bestandteile in der Membran, und zwar umso stärker, je größer der Transmembrandruck (der mittlere Druck über die gesamte Membranfläche entlang des Stoffstroms) ist. (Un)Polare Lösungsmittel waschen (un)polare Stoffe aus der Membran aus.
Beschichtete Membranen bieten neue Anwendungsmöglichkeiten der Membranfiltration, z. B. die Membranchromatographie. Die Membranen werden chemisch (z. B. mit C18, C8, n-Hexan, oder Sulfonsäureresten) beschichtet. Die dadurch veränderte Membranchemie soll die Membranen mit den Eigenschaften der Säulen aus der Chromatographie verbinden.[4]
Trennprinzip
Man unterscheidet die Membrantrennverfahren nach der treibenden Kraft, die der Trennung zugrunde liegt.
Druckgetriebene Prozesse


- Mikrofiltration
- kalte Sterilisation
- Entkeimung von Fruchtsäften, Wein und Bier
- Herstellung von aufgereinigtem Wasser
- Abtrennung von kolloidalen Oxiden oder Hydroxiden
- Trennung von Öl-Wasser-Emulsionen
- Entwässerung von Latices
- Abwasserbehandlung
- Biotechnologie (Ernten von Zellen)
- Ultrafiltration[1]
- Abtrennung von Proteinen (beispielsweise aus Milch)
- kalte Sterilisation in der Pharmazie (Antibiotikaproduktion)[5]
- Metall-Rückgewinnung und Abwasserreinigung in der Metallurgie
- Lebensmittelbehandlung (Produktion von „PRO-CAL“ einem Milchprodukt, das wenig Fett, aber viel Protein und Calcium enthält)
- Abtrennung von Partikeln, Mikroorganismen, Trubstoffen bei der Wasseraufbereitung aus Quellwässern oder Oberflächenwässern
- Membranreaktor
- Membranbelebungsreaktor (MBR)
- Nanofiltration
- Hyperfiltration = Umkehrosmose
- Wasser-Entsalzung (Trinkwassergewinnung aus Meerwasser oder Brackwasser)
- Aufkonzentrierung von Säften oder Milch
- Herstellung von ultra-reinem Wasser
- Einengen bei großtechnischen Prozessen
Eine Sonderform der druckgetriebenen Prozesse stellt die Diafiltration dar.
Konzentrationsgetriebene Prozesse
- Gastrennung
- Pervaporation
- Dialyse
- selektive Trennungen mit Flüssigmembranen
- Künstliche Lunge
Thermisch getriebene Prozesse
- Membrandestillation
- Thermoosmose (Thermodiffusion über Membranen)
Elektrisch getriebene Prozesse
- Elektrodialyse (siehe Dialyse (Chemie))
- Elektrodeionisation
- Chloralkali-Elektrolyse
- Natronlauge-Schwefelsäure Prozess
- Elektrofiltration
- Brennstoffzelle
Porengröße und Selektivität
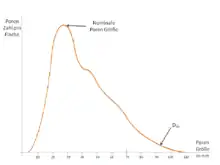
Die Porengrößen technischer Membranen werden je nach Hersteller sehr unterschiedlich angegeben. Eine gängige Form ist die Nominale Porengröße. Sie beschreibt das Maximum in der Porengrößenverteilung[6] und trifft nur eine ungenaue Aussage über das Rückhaltevermögen einer Membran. Die Ausschlussgrenze oder auch „Cut-off“ der Membran wird üblicherweise in Form des NMWC (englisch: Nominal Molecular Weight Cut-Off, auch MWCO, Molecular Weight Cut Off, Einheit: Dalton) angegeben. Er wird definiert als die minimale Molekülmasse eines globulären Moleküls, welches durch die Membran zu 90 % zurückgehalten wird. Der Cut-off kann je nach Bestimmungsmethode in den sogenannten D90 umgerechnet werden, der dann in einer metrischen Einheit angegeben wird. In der Praxis sollte der NMWC mindestens 20 % niedriger sein als die Molmasse des abzutrennenden Moleküls.
Filtermembranen werden nach ihrer Porengröße in vier Klassen eingeteilt:
| Porengröße | Molekülmasse | Verfahren | Filtrationsdruck | abgetrennt werden |
|---|---|---|---|---|
| > 10 µm | Filter | |||
| > 0,1 µm | >5000 kDa | Mikrofiltration | < 2 bar | Bakterien, Hefen, Partikel |
| 100–2 nm | 5–5000 kDa | Ultrafiltration | 1–10 bar | Makromoleküle, Proteine |
| 2–1 nm | 0,1–5 kDa | Nanofiltration | 3–20 bar | Viren, 2-wertige Ionen[7] |
| < 1 nm | < 100 Da | Umkehrosmose | 10–80 bar | Salze, kleine organische Moleküle |
Form und Gestalt der Membranporen hängen sehr vom Herstellungsverfahren ab und sind oft nur schwer spezifizierbar. Zur Charakterisierung führt man daher Testfiltrationen durch und bezeichnet als Porendurchmesser die Durchmesser der kleinsten Teilchen, welche die Membran nicht passieren konnten.
Der Rückhalt kann auf verschiedene Weisen bestimmt werden und stellt immer eine indirekte Messung der Porengröße dar. Eine Möglichkeit ist die Filtration von Makromolekülen (oft Dextran, Polyethylenglycol oder Albumin) und die Messung des Cut-offs mittels Gel-Permeations-Chromatographie. Diese Verfahren finden vor allem bei der Vermessung von Ultrafiltrationsmembranen Anwendung. Eine weitere Methode sind Testfiltrationen mit Partikeln definierter Größe und deren Messung mit Partikel Sizern oder Laser induzierte Breakdown Detektion (LIBD). Eine sehr anschauliche Charakterisierung ist die Messung des Rückhalts von Dextranblau oder anderen farbigen Molekülen. Auch der Rückhalt von Bakteriophagen oder Bakterien kann mit dem sogenannten „Bacteria-Challenge-Test“ Aussagen über die Porengröße liefern.
| Nominale Porengröße | Mikroorganismus | ATCC-Stamm Nummer |
|---|---|---|
| 0,1 µm | Acholeplasma laidlawii | 23206 |
| 0,3 µm | Bacillus Subtilis Sporen (!) | 82 |
| 0,5 µm | Pseudomonas diminuta | 19146 |
| 0,45 µm | Serratia marcescens | 14756 |
| 0,65 µm | Lactobacillus brevis |
Zur Bestimmung des Porendurchmessers gibt es physikalische Methoden wie die Quecksilberporosimetrie, Flüssig-Flüssig-Porosimetrie und Blaspunkt-Messung, die jedoch eine bestimmte Form der Poren (wie zylinderförmig oder aneinandergereihte sphärische Löcher) voraussetzen. Werden solche Verfahren für Membranen verwendet, deren Porengeometrie nicht den Idealvorstellungen entspricht, erhält man „nominelle“ Porendurchmesser, welche die Membran zwar charakterisieren, aber nicht notwendigerweise ihr tatsächliches Filtrationsverhalten und ihre Selektivität widerspiegeln.
Die Selektivität ist neben der Porengröße sehr stark abhängig von dem Trennverfahren, der Zusammensetzung der Membran und ihren elektrochemischen Eigenschaften. Durch eine hohe Selektivität können in der Kerntechnik Isotope angereichert (Uran-Anreicherung) und in der Industrie gasförmiger Stickstoff gewonnen (Gastrennung) werden. Im Idealfall können mit einer geeigneten Membran sogar Racemate angereichert werden.
Bei der Auswahl der Membran hat ihre Selektivität grundsätzlich Vorrang vor einer hohen Permeabilität, da sich niedrige Flüsse bei modularem Aufbau leicht durch Vergrößern der Filterfläche ausgleichen lassen. Für die Gasphase ist zu beachten, dass in einem Filtrationsprozess unterschiedliche Abscheidemechanismen wirken, so dass auch Partikel mit Größen weit unterhalb der Porengröße der Membran zurückgehalten werden können.
Auswahl und Auslegung einer Membrananlage
Die Auswahl der Membranen für eine gezielte Trennung basiert in der Regel auf einer Reihe von Anforderungen. Membranenanlagen müssen ausreichend Filterfläche bieten, um genügend große Mengen Feedlösung zu verarbeiten. Die ausgewählten Membranen müssen nicht nur hohe selektive Eigenschaften für die abzutrennenden Teilchen haben, sondern auch widerstandsfähig gegenüber Fouling sein und eine hohe mechanische Stabilität besitzen. Außerdem muss sie reproduzierbare Ergebnisse liefern und niedrige Herstellungskosten haben. Die Gleichung für die Modellierung der Dead-End Filtration bei konstantem Druckverlust wird durch das Darcy-Gesetz beschrieben.
Mit
- Vp – Permeiertes Volumen; [Vp] = m³
- t – Zeit; [t] = s
- Q – Volumenstrom; [Q] = m³/s
- Δp – Druckdifferenz;
- – Dynamische Viskosität des permeierenden Fluids; [] = Ns/m²
- A – durchströmte Fläche; [A] = m²
- Rm – membraneigener Widerstand;
- Rp – Gelpolarisationswiderstand;
Während Rm als reiner Übergangswiderstand zwischen Membran und Permeat als konstant angenommen werden kann, verändert sich Rp und nimmt mit wachsender Deckschicht zu. Das Darcy-Gesetz ermöglicht die Berechnung der Membraneigenschaften für eine gezielte Trennung zu bestimmten Bedingungen. Der Siebkoeffizient (oder Trennfaktor) ist definiert durch die Gleichung:
Cf und Cp sind die Konzentrationen in Feed und Permeat. Die hydraulische Durchlässigkeit ist definiert als der Kehrwert des Widerstands und wird vertreten durch die Gleichung:
wobei J der Permeat-Volumenstrom pro Einheit Membranfläche ist. Der Siebkoeffizient und die hydraulische Durchlässigkeit ermöglichen die schnelle Beurteilung der Membranleistung.
Geschichte
- 1748 erfolgten die ersten belegten Beobachtungen zur selektiven Permeabilität von Membranen durch Jean-Antoine Nollet, als er mit einer Schweinsblase als Trennmedium zwischen Wasser und Wein experimentierte. Er beobachtete dabei, wie sich die Blase unter dem Ausgleich des osmotischen Drucks langsam aufblähte, bis sie schließlich platzte.
- 1828 beschrieb Henri Dutrochet als erster das Osmometer.
- 1861 entdeckte Thomas Graham die chemische Dialyse: Während gelöste Stoffe die Membranen durchwandern, werden die Kolloide aufgehalten.
- 1864 stellte Moritz Traube erstmals künstliche, semipermeable Membranen dar, die er als Molekülsiebe erkannte. Sie wurden von Wilhelm Pfeffer und Jacobus Henricus van ’t Hoff für ihre Versuche verwendet
- 1916 erfand Richard Zsigmondy gemeinsam mit Wilhelm Bachmann den Membranfilter und Ultrafeinfilter. Diese Filter wurden zuerst ab 1917 von der Firma de Haën (später Riedel-de Haën) in Seelze produziert, später von der Göttinger Membranfiltergesellschaft mbH (heute Teil der Sartorius AG).
- 1924 führte Georg Haas die erste Blutwäsche außerhalb des Körpers durch.
- 1945 wurde der erste Mensch mit der von Willem Kolff entwickelten künstlichen Niere gerettet.
- 1949 entwickelten Sidney Loeb und Srinivasa Sourirajan an der University of California, Los Angeles die erste Umkehrosmose Membran, und brachten das Prinzip nach 8-jähriger Entwicklung zur Produktreife.
Membranentwicklung
Wichtigste Forschungszentren auf dem Gebiet der Stofftrennung mit Membranen in Europa sind das GKSS-Forschungszentrum Geesthacht, die Universitäten Twente-Enschede, Aachen und Kalabrien und das „Institut Européen des Membranes (IEM UMR)“ in Montpellier.
Siehe auch
Literatur
- Munir Cheryan: Handbuch Ultrafiltration. Behr, 1990, ISBN 3-925673-87-3.
- Eberhard Staude: Membranen und Membranprozesse. VCH, 1992, ISBN 3-527-28041-3.
- Marcel Mulder: Basic Principles of Membrane Technology. Kluwer Academic Publishers, 1996, ISBN 978-0-7923-4248-9.
- Thomas Melin, Robert Rautenbach: Membranverfahren. Springer, 2007, ISBN 3-540-00071-2.
Einzelnachweise
- Skript-TC4-Ultrafiltration Uni-Paderborn (PDF (Memento vom 2. April 2015 im Internet Archive)).
- Eric Baer: Hochentwickelte Polymere, Spektrum der Wissenschaften, 12/1986, S. 150.
- GE Healthcare, Evonik, Koch, Mycrodin Nadir,Toray, Alfa Laval (Memento vom 6. Juni 2013 im Internet Archive), Sterlitech.
- Handbook of Membrane Separations, Edited by Anil K.Pabby, Syed S.H.Rizvi, Ana aria Sastre, CRC Press, ISBN 978-0-8493-9549-9.
- S. Ebel und H. J. Roth (Herausgeber): Lexikon der Pharmazie, Georg Thieme Verlag, 1987, S. 421, ISBN 3-13-672201-9.
- TU Berlin Skript – 2 Grundlagen der Membranprozesse (Archivierte Kopie (Memento vom 16. April 2014 im Internet Archive); PDF-Datei; 6,85 MB) Seite 6.
- Erfahrungen und Anwendungspotential der Nanofiltration – Uni Linz (PDF (Memento vom 5. April 2013 im Internet Archive)).