Kaliumperiodat
Kaliumperiodat ist eine chemische Verbindung aus der Gruppe der Periodate (genauer das Kaliumsalz der Metaperiodsäure). Es ist ein weißer, kristalliner Feststoff, der sich in Wasser relativ schlecht löst.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
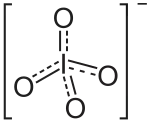 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Kaliumperiodat | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | KIO4 | ||||||||||||||||||
| Kurzbeschreibung |
farb- und geruchloser Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 230,00 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
3,62 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
5,1 g·l−1 bei 25 °C in Wasser[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Zur Darstellung im Labor verwendet man Kaliumiodat, das mithilfe von Kaliumperoxodisulfat im Alkalischen (zweckmäßigerweise in Kalilauge, KOH) oxidiert wird:
Die Reaktion wird in siedender Lösung durchgeführt. Danach kann das Salz mittels Neutralisation mit halbkonzentrierter Salpetersäure ausgefällt, mit Eiswasser gewaschen und abfiltriert werden. Eine andere Möglichkeit ist das Einleiten von Chlor in alkalische Kaliumiodatlösung.[3][4]:
Eigenschaften
Kaliumperiodat ist ein starkes Oxidationsmittel. So wird eine wässrige Lösung von Kaliumiodid von Kaliumperiodat zum elementaren Iod oxidiert, Mangan(II)-Salze werden zu Permanganaten oxidiert.[5]
Seine Kristalle sind isomorph mit Kaliumperchlorat. Beim Auflösen in Kalilauge entsteht Kaliumdiperiodat[4], das mit Salpetersäure wieder zum einfachen Kaliumperiodat rückgeführt werden kann.[5][6]
Kaliumorthoperiodat K2H3IO6, das durch Oxidation von Kaliumiodat mit Natriumhypochlorit entsteht[5], gibt bei 100 °C Wasser ab und geht in Kaliumdiperiodat über.[7]
In wässrigen Lösungen von Periodaten liegen folgende Gleichgewichte vor:[5]
Verwendung
Neben seiner Wirkung als Oxidationsmittel wird Kaliumperiodat als Reagenz zur analytischen Bestimmung von Cer verwendet.[8]
Einzelnachweise
- Datenblatt Kaliumperiodat bei Alfa Aesar, abgerufen am 5. November 2021 (Seite nicht mehr abrufbar).
- Claudia Synowietz (Hrsg.): Taschenbuch für Chemiker und Physiker. Begründet von Jean d’Ans, Ellen Lax. 4. Auflage. Band 2: Organische Verbindungen. Springer, Berlin 1983, ISBN 3-540-12263-X.
- G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 325.
- C. Rammelsberg: "Ueber die Ueberjodsäure und ihre Salze" in Ber. d. dt. chem. Ges. 1868, A1, S. 70ff. Volltext
- C. E. Housecroft, A. G. Sharpe: "Inorganic chemistry", Verlag Pearson Education, 2005, ISBN 978-0-13-039913-7. S. 487 (eingeschränkte Vorschau in der Google-Buchsuche)
- B. Brehler, H. Jacobi, H. Siebert: "Kristallstruktur und Schwingungsspektrum von K4J2O9" in Zeitschrift für anorganische und allgemeine Chemie 1968, 362(5-6), S. 301–311. doi:10.1002/zaac.19683620510
- N. I. Nikitina,Z. K. Nikitina: "Thermolysis of disubstituted lithium and sodium orthoperiodates" in Russian Journal of Inorganic Chemistry 2007,52(4), S. 535–541. doi:10.1134/S0036023607040031
- M. Venugopalan and K. J. George: "Determination of cerium by potassium periodate" in Naturwissenschaften, 43(15), S. 348–349. doi:10.1007/BF00755157

