Isobornylacetat
Isobornylacetat ist eine chemische Verbindung aus der Gruppe der Carbonsäureester und ist isomer zu Essigsäurebornylester. Es kommt in einer Reihe von ätherischen Ölen vor[6] und ist der Ethylester des Terpens Isoborneol.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
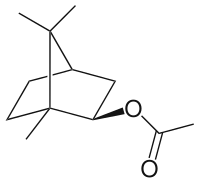 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Isobornylacetat | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Summenformel | C12H20O2 | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit charakteristischem Geruch[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 196,29 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
0,98 g·cm−3[2] | |||||||||||||||
| Siedepunkt |
215 °C[2] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Brechungsindex |
1,4635 (20 °C)[4] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Isomere
Isobornylacetat ist immer exo-konfiguriert, die endo-Konfiguration wird als Bornylacetat bzw. Essigsäurebornylester bezeichnet. Es existieren zwei isomere Formen, (−)- und (+)-Isobornylacetat [Synonyme: (1S,2S,4S)- bzw. (1R,2R,4R)-Bornylacetat], die häufig als 1:1-Gemisch (Racemat) vorkommen.
Gewinnung und Darstellung
Isobornylacetat wird aus Camphen dargestellt, wobei pro Jahr mehr als 1000 Tonnen produziert werden.[3]
Eigenschaften
Isobornylacetat ist eine farblose bis gelbliche Flüssigkeit mit charakteristischem Geruch, welche sehr schlecht löslich in Wasser ist. Sie besitzt eine dynamische Viskosität von 8,5 mPa·s bei 20 °C.[2]
Verwendung
Isobornylacetat ist in Riechstoffkompositionen (Badepräparate, Seifenparfüms, Sprays) enthalten und dient als Zwischenprodukt bei der Herstellung von Campher.[2]

Sicherheitshinweise
Die Dämpfe von Isobornylacetat können mit Luft ein explosionsfähiges Gemisch (Flammpunkt 88 °C, Zündtemperatur 430 °C) bilden.[2]
Einzelnachweise
- Eintrag zu ISOBORNYL ACETATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 11. Dezember 2021.
- Eintrag zu Isobornylacetat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Februar 2017. (JavaScript erforderlich)
- Toxikologische Bewertung von Isobornylacetat (PDF) bei der Berufsgenossenschaft Rohstoffe und chemische Industrie (BG RCI), abgerufen am 26. August 2010.
- Datenblatt Isobornyl acetate bei Sigma-Aldrich, abgerufen am 26. August 2010 (PDF).
- Datenblatt Isobornylacetat bei Merck, abgerufen am 6. April 2011.
- Karl‐Georg Fahlbusch, Franz‐Josef Hammerschmidt, Johannes Panten, Wilhelm Pickenhagen, Dietmar Schatkowski, Kurt Bauer, Dorothea Garbe, Horst Surburg: Flavors and Fragrances. In: Ullmann’s Encyclopedia of Industrial Chemistry. Band 15, 2012, S. 111, doi:10.1002/14356007.a11_141.
