Indigoidin
Indigoidin ist eine organische Verbindung der Gruppe der Azachinone. Es ist ein blaues Pigment, das einige Bakterienarten bilden und in das umgebende Medium ausscheiden.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
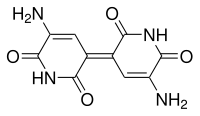 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Indigoidin | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C10H8N4O4 | ||||||||||||
| Kurzbeschreibung |
blaues Pulver[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 248,19 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Löslichkeit | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Geschichte
Otto Voges erforschte und beschrieb bereits im Jahr 1893 in Kiel die Bakterienart Bacillus indigoferus, umbenannt nach ihm Vogesella indigofera, die das umgebende Medium (Wasser) kontinuierlich von leicht bläulich (24 Stunden) bis zu Königsblau (48 Stunden) verfärbte.
Der Nobelpreisträger Richard Kuhn und Mitarbeiter publizierten in den Jahren 1964 und 1965 einige Artikel in der Fachpresse über das Vorkommen, die Struktur und Synthese von Indigoidin.[4][5][6]
Im Jahr 1979 beschrieben Carl-Gerd Dieris und H.-D. Scharf die synthetische Herstellung von Indigoidin.[7]
Vorkommen
Die Indigoidin kommt bei folgenden Arten von Bakterien vor:
- Arthrobacter atrocyaneus
- Arthrobacter crystallopoietes
- Arthrobacter polychromogones
- Corynebacterium insidiosum
- Erwinia chrysanthemi umbenannt Dickea dadantii
- Vogesella indigofera vormals Bacillus indigoferus und Pseudomonas indigofera
Gewinnung und Herstellung
Indigoidin kann synthetisch aus Citrazinsäure (C6H5NO4) hergestellt werden, die aus Citronensäure und Ammoniak leicht zugänglich ist.
Biosynthese
Die Biosynthese von Indigoidin geht von Glutamin aus, das enzymatisch oxidiert, zum Heterocyclus cyclisiert und dimerisiert wird.[8]
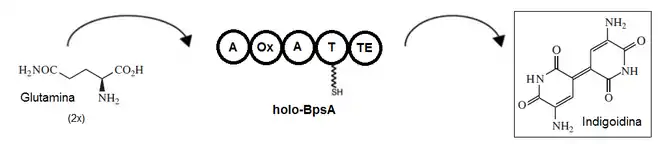
Die Angaben der Segmente A, Ox, A, T und Te beziehen sich auf definierte Domainen innerhalb der Enzymstruktur des bpsA-Genprodukts BPSA.[9]
Eigenschaften
Physikalische Eigenschaften
Indigoidin ist ein blaues amorphes Pulver mit der molaren Masse von 248,19 g·mol−1. Es ist in Wasser und den meisten anderen Lösungsmitteln unlöslich, löst sich jedoch in 6 n Salzsäure mit königsblauer Farbe sowie in heißer Schwefelsäure mit orangebrauner Farbe auf.[2]
Chemische Eigenschaften
Die Farbigkeit von Indigoidin wird auf ein indigoides Chromophor zurückgeführt. Die NMR-spektroskopischen Untersuchungen an Derivaten bestätigten die angegebene symmetrische Struktur. Die Stickstoffatome in den chinoiden Ringen wegen wird Indigoidin der Verbindungsklasse der Azachinone zugeordnet.
Derivate
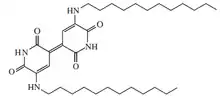
Ein Derivat ist der violette Farbstoff N5,N5′-Didodecylindigoidin, (C34H56N4O4), der aus dem psychrophilen Bakterium Shewanella violacea DSS12 isoliert wurde.[10]
Siehe auch
- Indigo – C16H10N2O2
- Indigotin I – C16H8N2Na2O8S2
- Königsblau – anorganische Pigmente
Literatur
- Carl-Gerd Dieris: Zur Frage der Luminiszenz von thermooxidativ geschädigten Polycarpolaktam. Eine neue Synthese des Bakterienfarbstoffes Indigoidin und seiner Tetra-N-alkylderivate. 1980.
- Hans Günter Schlegel: Allgemeine Mikrobiologie. Thieme Verlagsgruppe, Stuttgart 1992, ISBN 978-3-13-444607-4.
- Sylvie Reverchon, Carine Rouanet, Dominique Expert, William Nasser: Characterization of Indigoidine Biosynthetic Genes in Erwinia chrysanthemi and Role of This Blue Pigment in Pathogenicity. In: Journal of Bacteriology. Band 184, Nr. 3, 2. Januar 2002, S. 654–665, doi:10.1128/JB.184.3.654-665.2002, PMID 11790734.
- Christin Schönfeld: Charakterisierung und biochemische Analyse der Indigoidin Synthease BpsA aus S. lavendulae ATCC 11924. Masterarbeit, Philipps-Universität Marburg 2012.
- M. Müller, S. Ausländer, D. Ausländer, C. Kemmer, M. Fussenegger: A novel reporter system for bacterial and mammalian cells based on the non-ribosomal peptide indigoidine. Metabolic Engineering 14/2012, S. 325–335 (doi:10.1016/j.ymben.2012.04.002).
- H. Kobayashi, Y. Nogi, K. Hirokoshi: New violet 3,3’-bipyridyl pigment purified from deep-sea microorganism Shewanella violacea DSS12. In: Extremophiles Nr. 11(2)/2012, S. 245–250. PMID 17102923.
Einzelnachweise
- R. A. Abramovitch: The Chemistry of Heterocyclic Compounds. Pyridine and Its Derivatives. John Wiley & Sons, New York 1974, ISBN 0-471-37915-8, S. 860.
- Eintrag zu Indigoidin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 11. November 2014.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Richard Kuhn, Helmut Bauer, Hans-Joachim Knackmuss, Daisy A. Kuhn, Mortimer P. Starr: Die Struktur der blauen Pigmente von Corynebacterium insidiosum, Arthrobacter atrocyaneus, Pseudomonas indigofera und Arthrobacter crystallopoietes. In: Naturwissenschaften. Band 51, Nr. 17, 1. Januar 1964, S. 409, doi:10.1007/BF00609040.
- Richard Kuhn, Helmut Bauer, Hans-Joachim Knackmuss: Struktur und Synthesen des Bakterienfarbstoffs Indigoidin. In: Chemische Berichte. Band 98, Nr. 7, 1965, S. 2139–2153, doi:10.1002/cber.19650980714.
- Richard Kuhn, Mortimer P. Starr, Daisy A. Kuhn, Helmut Bauer, Hans-Joachim Knackmuss: Indigoidine and other bacterial pigments related to 3,3’-bipyridyl. In: Archiv für Mikrobiologie. Band 51, Nr. 1, 1. März 1965, S. 71–84, doi:10.1007/BF00406851.
- C.-G. Dieris, H.-D. Scharf: Eine neue Synthese des Bakterienfarbstoffs Indigoidin und seiner Tetra-N-alkyl-Derivate. In: Synthesis. Band 1979, Nr. 12, 1979, S. 948–950, doi:10.1055/s-1979-28883.
- M. Müller, S. Ausländer, D. Ausländer, C. Kemmer, M. Fussenegger: A novel reporter system for bacterial and mammalian cells based on the non-ribosomal peptide indigoidine. In: Metabolic Engineering. Nr. 14, 2012, S. 325–335, doi:10.1016/j.ymben.2012.04.002.
- Hitoshi Takahashi, Takanori Kumagai, Kyoko Kitani, Miwako Mori, Yasuyuki Matoba and Masanori Sugiyama: Cloning and Characterization of a Streptomyces Single Module Type Non-ribosomal Peptide Synthetase Catalyzing a Blue Pigment Synthesis, J. Biol. Chem. 282 (12), S. 9073–9081 (2007).
- H. Kobayashi, Y. Nogi, K. Hirokoshi: New violet 3,3’-bipyridyl pigment purified from deep-sea microorganism Shewanella violacea DSS12. In: Extremophiles. Nr. 11(2), 2007, S. 245–250.