Griseofulvin
Griseofulvin ist eine natürlich vorkommende chemische Verbindung aus der Gruppe der Schimmelpilzgifte (Mykotoxine). Es wird als Arzneistoff in der Behandlung von Hautinfektionen und -pilzen eingesetzt und ist oral wirksam. Chemisch handelt es sich beim Griseofulvin um einen Abkömmling (Derivat) des Benzofurans.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
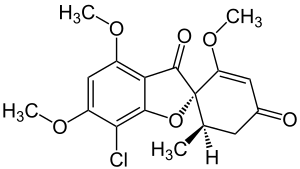 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Griseofulvin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C17H17ClO6 | |||||||||||||||||||||
| Kurzbeschreibung |
weißer geruchsloser Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse |
oral wirksames Antimykotikum | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 352,77 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser (8,64 mg·l−1 bei 25 °C)[3] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Geschichte
Griseofulvin wurde 1939 in Kulturen von Penicillium griseofulvum entdeckt.[7][8] Die Konstitution der Verbindung wurde erst 1952 aufgeklärt.[9] Mittels Röntgenstrukturanalyse wurde 1977 die absolute Konfiguration bestimmt.[10]
Vorkommen
Neben dem Penicillium griseofulvum kommt Griseofulvin auch in Penicillium nigricans und Aspergillus lanosus vor. Es besitzt antimykotische Wirkung gegenüber Dermatophyten (Fadenpilze). Gegen andere Pilze wie z. B. Schimmelpilze ist es unwirksam.[6]
Darstellung und Gewinnung
Die technische Herstellung von Griseofulvin erfolgt durch Fermentation bei 25 °C mit Penicillium patulum in pH-geregelten und gut belüfteten Kulturen mit relativ hohen Kohlenhydratkonzentrationen. Die Isolierung erfolgt nach Abtrennung des Mycels durch eine Extraktion mit organischen Lösungsmitteln, wie z. B. Butylacetat.[6]
Eigenschaften
Griseofulvin ist eine feste kristalline Substanz. Sie tritt in drei polymorphen Formen auf, die sich in ihren Schmelzpunkten unterscheiden.[2] Die thermodynamisch stabile und pharmazeutisch angewendete Form ist das Polymorph I. Die Formen II und III konnten nur durch eine Kristallisation aus der Schmelze gewonnen werden.[2]
| Polymorphe Form | Schmelzpunkt (K) |
Schmelzpunkt (°C) |
Spezifische Schmelzenthalpie (J·g−1) |
Molare Schmelzenthalpie (kJ·mol−1) |
Dichte (g·cm−3) |
|---|---|---|---|---|---|
| Form I | 492 | 219 | 116 | 40,9 | 1,459 |
| Form II | 486 | 213 | 82 | 28,9 | 1,358 |
| Form III | 477 | 204 | 78 | 27,5 | |
Die Sublimationsdruckfunktion der Form I ergibt sich nach August entsprechend ln(P) = A−B/T (P in Pa, T in K) mit A = 35,27 und B = 15,995 im Temperaturbereich von 421,15 bis 445,15 K. Der Sublimationsdruck beträgt bei 148 °C 6,81·10−2 Pa, bei 172 °C 0,528 Pa. Hier ergibt sich eine mittlere Sublimationsenthalpie von 133,0 kJ·mol−1.[11]
Wirkungsmechanismus
Griseofulvin zeigt eine anti-proliferative Wirkung bei verschiedenen Krebszellen und inhibiert das Tumorwachstum von athymischen Mäusen. In vitro wird die Induktion von Apoptose bei Krebszellen beobachtet,[12] während normale Zellen davon nicht betroffen sind.[13][14][15][16][17]
Unerwünschte Wirkungen
Überdosiert kann Griseofulvin zu Schlafstörungen, Schwindel und Kopfschmerz führen. Auch rheumatische Nebenwirkungen sind beobachtet worden. Die Wirksamkeit anderer Medikamente oder von Kontrazeptiva kann (durch Enzyminduktion verschiedener Cytochrom-P450-Isoenzyme[18]) herabgesetzt werden.[19]
Strukturverwandte Naturstoffe
Es existieren mit Griseofulvin strukturverwandte Naturstoffe. Das Isogriseofulvin und das Epigriseofulvin werden aus Penicillium-Kulturen, das 7-Dechlorogriseofulvin aus Nigrospora-Kulturen gewonnen. 7-Brom-7-dechlorgriseofulvin entsteht, wenn Kulturen von Penicillium griseofulvum oder Penicillium nigricans Kaliumbromid zugegeben wird.[6]
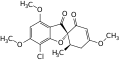 Isogriseofulvin
Isogriseofulvin Epigriseofulvin
Epigriseofulvin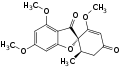 7-Dechlorogriseofulvin
7-Dechlorogriseofulvin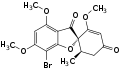 7-Bromo-7-dechlorogriseofulvin
7-Bromo-7-dechlorogriseofulvin
Handelsnamen
Sanofi: Likuden (D, außer Handel). Fertigpräparate gibt es in den deutschsprachigen Ländern nicht mehr im Markt.
Einzelnachweise
- Datenblatt Griseofulvin bei Alfa Aesar, abgerufen am 22. März 2010 (Seite nicht mehr abrufbar).
- Yuan Su; Jia Xu; Qin Shi; Lian Yub; Ting Cai: Polymorphism of griseofulvin: concomitant crystallization from the melt and a single crystal structure of a metastable polymorph with anomalously large thermal expansion in Chem. Commun. 54 (2018) 358–361, doi:10.1039/C7CC07744K, Electronic Supplementary Information (pdf).
- Eintrag zu Griseofulvin in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar)
- Datenblatt Griseofulvin from Penicillium griseofulvum bei Sigma-Aldrich, abgerufen am 3. April 2011 (PDF).
- A. Kleemann, J. Engel, B. Kutscher, D. Reichert: Pharmaceutical Substances - Synthesis, Patents, Applications, 4. Auflage (2001) Thieme-Verlag Stuttgart, ISBN 978-1-58890-031-9.
- Eintrag zu Griseofulvin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 21. Oktober 2022.
- Oxford, A.E.; Raistrick, H.; Simonart, P.: Studies in the biochemistry of micro-organisms: Griseofulvin, C17H17O6Cl, a metabolic product of Penicillium griseofulvum Dierckx in Biochem. J. 33 (1939) 240–248, doi:10.1042/bj0330240.
- Karl Wurm, A. M. Walter: Infektionskrankheiten. In: Ludwig Heilmeyer (Hrsg.): Lehrbuch der Inneren Medizin. Springer-Verlag, Berlin/Göttingen/Heidelberg 1955; 2. Auflage ebenda 1961, S. 9–223, hier: S. 55.
- Grove, J.F.; MacMillan, J.; Mulholland, T.P.C.; Rogers, M.A.T.: 759. Griseofulvin. Part I in J. Chem. Soc. 1952, 3949–3958, doi:10.1039/jr9520003949.
- Malmros, G.; Wagner, A.; Maron, L.: (2S,6′R)-7-chloro-2′,4,6,-trime-thoxy-6′-methyl-spiro-(benzofuran-2(3H),2-(2′)cyclohexene)-3,4′-dione C17H17O6Cl in Cryst. Struct. Commun. 6 (1977) 463–470.
- Blokhina, S.; Sharapova, A.; Ol’khovich, M.; Perlovich, G.: Thermal behavior of griseofulvin: fusion, sublimation and vaporization in J. Therm. Anal. Calorim. 147 (2022) 11195–11204.
- Y. H. Uen u. a.: NF-kappaB pathway is involved in griseofulvin-induced G2/M arrest and apoptosis in HL-60 cells. In: J Cell Biochem 101, 2007, S. 1165–1175, PMID 17226769.
- B. Rebacz u. a.: Identification of griseofulvin as an inhibitor of centrosomal clustering in a phenotypebased screen. In: Cancer Res 67, 2007, S. 6342–6350, PMID 17616693.
- Y. S. Ho u. a.: Griseofulvin potentiates antitumorigenesis effects of nocodazole through induction of apoptosis and G2/M cell cycle arrest in human colorectal cancer cells. In: Int J Cancer 91, 2001, S. 393–401, PMID 11169965.
- D. Panda u. a.: Kinetic suppression of microtubule dynamic instability by griseofulvin: implications for its possible use in the treatment of cancer. In: PNAS 102, 2005, S. 9878–9883, PMID 15985553; PMC 1174985 (freier Volltext).
- P. Singh u. a.: Microtubule assembly dynamics: An attractive target for anticancer drugs. In: IUBMB Life 60, 2008, S. 368–375, PMID 18384115.
- K. Rathinasamy u. a.: Griseofulvin stabilizes microtubule dynamics, activates p53 and inhibits the proliferation of MCF-7 cells synergistically with vinblastine. (PDF; 2,7 MB) In: BMC Cancer 10, 2010, 213, doi:10.1186/1471-2407-10-213.
- Torsten Kratz, Albert Diefenbacher: Psychopharmakotherapie im Alter. Vermeidung von Arzneimittelinteraktionen und Polypharmazie. In: Deutsches Ärzteblatt. Band 116, Heft 29 f. (22. Juli) 2019, S. 508–517, S. 510.
- Likuden M 500 mg - Patienteninformationen, Beschreibung, Dosierung und Richtungen. Abgerufen am 19. Juni 2018.