Fumagillin
Fumagillin ist ein komplexes Biomolekül, vom Sesquiterpen-Typ.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
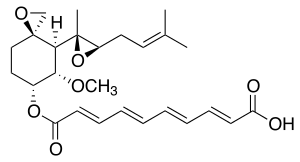 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Fumagillin | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C26H34O7 | |||||||||||||||||||||
| Kurzbeschreibung |
hellgelbe Nadeln[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
P01AX10 | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 458,54 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Vorkommen

In der Natur kommt es in Aspergillus fumigatus und in Penicillium nigricans vor.[1]
Anwendung
In Nordamerika ist es in verschiedenen Formen zugelassen und wird bei Mikrosporidiose eingesetzt.[1] Eine topische Anwendung kann bei mikrosporidialer Keratokonjunktivitis erfolgen. Bei Nosemose wird es in Zuckersirup gemischt.
Wirkungen gegen Malaria, Amöben, Leishmanien und Trypanosomen sowie gegen Neovaskularisation sind nachgewiesen und befinden sich derzeit in weiterer Erforschung.
Wirksamkeit
Fumagillin bindet über das Spiroepoxid irreversibel an eine Histidingruppe von Methionin-Aminopeptidasen (MetAP)[1], die neu synthetisierte Proteine um die dem Start-codon entsprechende N-terminale Methioningruppe verkürzen. Da dieser Schritt für die Biosynthese funktionaler Proteine essentiell ist, sterben Organismen mit nur einem Subtyp an MetAP. Aus diesem Grund werden MetAP-Inhibitoren und somit auch Fumagillin und seine Derivate unter anderem als potentielle Antibiotika erforscht. Es wurde des Weiteren beobachtet, dass Fumagillin beim Menschen, der zwei MetAP-Subtypen besitzt, die Angioneogenese hemmt,[4] was dazu geführt hat, dass Fumagillin und seine Derivate als Medikamente in der Krebstherapie erforscht wurden bzw. werden.[1]
Nebenwirkungen
Da Gewichtsverlust beobachtet wurde, wird an Derivaten geforscht. In klinischen Studien hat sich gezeigt, dass Fumagillin als Medikament zur Krebstherapie, aufgrund seiner hohen Neurotoxizität, ungeeignet ist, was zur Entwicklung von zahlreichen synthetischen und halbsynthetischen Derivaten geführt hat.[5]
Weiteres
Spaltet man von Fumagillin die saure Seitenkette ab, so resultiert der Alkohol Fumagillol, der immunsuppressiv wirkt.[1]
Handelsnamen
- Amebacillin, Fumagilin, Fumidil B
Literatur
- Antiparasitic activities of novel, orally available fumagillin analogs. In: Bioorganic & Medicinal Chemistry Letters 19 (2009) 5128–5131 (PDF; 399 kB; englisch)
- Apiculture Factsheet: Nosema, März 2012 (PDF; 113 kB; englisch)
- Fumagillin and Fumarranol Interact with P. falciparum Methionine Aminopeptidase 2 and Inhibit Malaria Parasite Growth In Vitro and In Vivo. In: Chemistry & Biology, Volume 16, Issue 2, 193-202, 27 February 2009, doi:10.1016/j.chembiol.2009.01.006
Weblinks
- Cytokines & Cells Encyclopedia – COPE: Fumagillin
Einzelnachweise
- Eintrag zu Fumagillin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 2. Juli 2019.
- Datenblatt Fumagillin from Aspergillus fumigatus bei Sigma-Aldrich, abgerufen am 2. April 2011 (PDF).
- Eintrag zu Fumagillin in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar)
- Ingber, D. E.; Fujita, T.; Kishmoto, S.; Sudo, K.; Kanamaru, T.; Brem, H.; Folkman, J.; Nature 1990, 345, 555.
- Exemplarisch werden hier nur TNP470: "Ingber, D.; Fujita, T.; Kishimoto, S.; Sudo, K.; Kanamaru, T.; Brem, H.; Folkman, J.; Nature 1990, 348, 555." und CKD-731: "Han, C. K.; Ahn S. K.; Bioorganic & Medicinal Chemistry Letters 2000, 10(1), 39-43." aufgeführt.